Vinylalkohol
| Vinylalkohol | |||
|---|---|---|---|
| IUPAC-navn Ethenol | |||
| Generelt | |||
| Andre navne | Hydroxyethen Hydroxyethylen | ||
| Molekylformel | C2H4O | ||
| Molarmasse | 44,053 g/mol | ||
| CAS-nummer | |||
| PubChem | |||
| SMILES | OC=C | ||
| InChI | 1S/C2H4O/c1-2-3/h2-3H,1H2 | ||
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |||
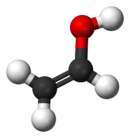
Vinylalkohol (IUPAC-navn: ethenol) er en alkohol med den kemiske formel CH2CHOH. Vinylalkohol er en isomer af acetaldehyd og ethylenoxid. Det kan dannes ved elimination af vand fra ethylenglykol ved en temperatur på 900 °C og lavt tryk.[1] Vinylalkohol er dog en ustabil forbindelse og vil efterhånden tautomerisere til det mere stabile acetaldehyd.
Tautomerisering mellem vinylalkohol og acetaldehyd
Under normale betingelser undergår vinylalkohol tautomerisering til acetaldehyd:
Ved stuetemperatur er acetaldehyd (H3CC(O)H) mere stabil end vinylalkohol (H2C=CHOH) med en energiforskel på 42,7 kJ/mol:[2]
- H2C=CHOH → H3CC(O)H ΔH298,g = −42,7 kJ/mol
Denne keto-enol-tautomerisering har en høj aktiveringsenergi og sker derfor ikke ved temperaturer nær stuetemperatur. Tautomerisering kan dog fremmes via fotokemiske processer, og vinylalkohol spiller muligvis en rolle i dannelsen af organiske syrer i atmosfæren.[3][4]
Polyvinylalkohol
På grund af vinylalkohols ustabilitet fremstilles termoplasttypen polyvinylalkohol (PVA eller PVOH) indirekte via polymerisering af vinylacetat efterfulgt af hydrolyse af esterbindingerne (Ac = acetyl, HOAc = eddikesyre):
- n CH2=CHOAc → (CH2−CHOAc)n
- (CH2−CHOAc)n + n H2O → (CH2−CHOH)n + n HOAc
Som ligand
Der findes mange kendte metalkomplekser, i hvilke vinylalkohol indgår som ligand. Et eksempel er Pt(acac)(η2-C2H3OH)Cl.[5]
Forekomst i det interstellare rum
Der er blevet fundet vinylalkohol i den molekylære tåge Sagittarius B ved hjælp af et 12-meters radioteleskop ved Kitt Peak National Observatory i Arizona, USA.[6] At vinylalkohol kan være stabil i det (foryndede) interstellare medium viser, at forbindelsens tautomerisering til acetaldehyd ikke foregår unimolekylært.
Referencer
- ^ Clayden, Jonathan; Greeves, Nick, og Warren, Stuart. Organic Chemistry, 2nd edition, pp. 456-57. Oxford University Press, 2012. ISBN 978-0-19-927029-3. (engelsk)
- ^ R.D. Johnson III. "CCCBDB NIST Standard Reference Database". Hentet 30. januar 2017. (engelsk)
- ^ (engelsk) Heazlewood, B. R.; Maccarone, A. T.; Andrews, D. U.; Osborn, D. L.; Harding, L. B.; Klippenstein, S. J.; Jordan, M. J. T.; Kable, S. H. "Near-threshold H/D exchange in CD3CHO photodissociation." Nat. Chem. 2011, 3, 443−448.
- ^ Andrews, D. U.; Heazlewood, B. R.; Maccarone, A. T.; Conroy, T.; Payne, R. J.; Jordan, M. J. T.; Kable, S. H. "Photo-tautomerization of acetaldehyde to vinyl alcohol: A potential route to tropospheric acids." Science 2012, 337, 1203−1206. (engelsk)
- ^ F. A. Cotton, J. N. Francis, B. A. Frenz, M. Tsutsui. "Structure of a dihapto(vinyl alcohol) complex of platinum(II)". Journal of the American Chemical Society, 1973, volume 95, pp. 2483-6. (engelsk)
- ^ "Scientists Toast the Discovery of Vinyl Alcohol in Interstellar Space". National Radio Astronomy Observatory. 1. oktober 2001. Hentet 30. januar 2017. (engelsk)
Se også
- Enol
- Ethanol
- Ethynol
Medier brugt på denne side
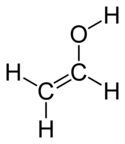
Structural formula of ethenol
Keto-enol tautomerism of ethanal and ethenol