Metan
| Metan | |
|---|---|
| Synonymer: | Biogas, Metylhydrid, Naturgas, Sumpgas |
| Sumformel: | CH4 |
| Strukturformel: |  |
| Kugleskalsmodel: |  |
| Fysiske egenskaber | |
| Molarmasse | 16,04246 g/mol |
| Smeltepunkt: | -182.5 °C (101,325 kPa) |
| Kogepunkt: | -161.5 °C (101,325 kPa) |
| Identitetsnummer | |
| CAS-nummer: | 74-82-8 |
Metan (methan) er den simpleste af millioner af mulige kulbrinteforbindelser – kemiske forbindelser mellem kulstof og brint. Ved stuetemperatur og atmosfærisk tryk er stoffet en gasart.
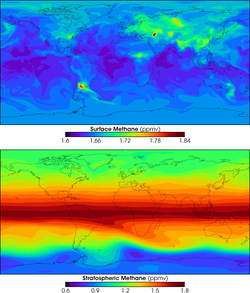

Metan dannes blandt andet som et slutprodukt fra anaerob nedbrydning af visse typer organisk materiale, hvorfor gassen også omtales som sumpgas eller biogas, men 80% af den metan der findes i miljøet, kommer fra menneskelige aktiviteter, primært fra landbrug.
Miljøforhold
Metan er en drivhusgas, som er omkring 25 gange mere effektiv til drivhuseffekten end carbondioxid (CO2).[1] I løbet af de sidste 200 år er atmosfærens metanindhold mere end fordoblet fra 0,8 til 1,7 ppm.
Den seneste globale temperaturstigning har betydet en begyndende optøning af den sibiriske tundra, hvor permafrost ellers har bundet enorme mængder af metan.[2] Metan og olie forekommer ofte sammen med andre gasser. Således er der fra Coal Oil Point, et offshore område ud for Santa Barbara i Californien, et udslip af metan på 40 ton pr dag. Store udslip truer også fra såkaldte "dødens søer" i Afrika, specielt Kivusøen, der skønnes at indeholde 65 km3 metan og 256 km3 kuldioxid.
Med sprængningerne af Nordstream gasledningerne i Østersøen skete der et udslip på størrelse med hele Danmarks eller hele Paris’ udslip på et år.[3]
Da metan indeholder kulstof C, er det vigtigt at have den med i sine betragtninger, når man vil forstå kulstofkredsløbet i naturen. Mange vådområder binder eksempelvis kuldioxid (CO2), men afgiver til gengæld metan (CH4). På trods af dette forhold, har undersøgelser dog vist, at vådområder er effektive netto C-lagre alt i alt.[4]
Rumobservatoriet EMIT er et “øje” på Den Internationale Rumstation, der bl.a. registrerer udledning af metan. Der er i 2022 allerede blevet identificeret mere end 50 superudledere af metan, deriblandt lossepladser og olie- og gasanlæg.[5][6]
Tekniske anvendelser
Metan bruges som energikilde, idét det er den primære bestanddel i naturgas. Metangas lugter i sig selv ikke af noget, så når gassen skal bruges som brændstof, tilsætter man en lille smule af en stærkt lugtende svovlforbindelse, f.eks. ætylmercaptan, så mennesker via deres lugtesans bliver advaret i tide om lækager.
Majskolber kan omdannes til kulstofbriketter, som kan lagre store mængder metangas ved lavt tryk.[7] Det kan anvendes i biler, hvor det lette metanlager fint kan være under et passagersæde.
Ved forbrænding frigøres der 890 kJ pr mol.
Se også
- Kulstofkredsløbet
- Kemiske stofgrupper
- Kryovulkan
- Miller-Urey-eksperimentet
Kilder/Referencer
- ^ 25 gange kraftigere end CO2: Stigende metan-udledning forvirrer forskere Emilie Aaagaard, 12. juni 2019 på dr.dk
- ^ SEA 'BOILING' WITH METHANE DISCOVERED IN SIBERIA: 'NO ONE HAS EVER RECORDED ANYTHING LIKE THIS BEFORE' Neewsweek 2019
- ^ »Kæmpestor« stigning af metan i atmosfæren efter Nord Stream-læk. Videnskab.dk 2022
- ^ Iowa State University (2008, May 8)
- ^ Methane 'super-emitters' on Earth spotted by space station experiment. Space.com 2022
- ^ EMIT Earth Surface Mineral Dust Source Investigation. Jet Propulsion Laboratory 2022
- ^ February 21, 2007, Science Daily: From Farm Waste To Fuel Tanks: Record-breaking Methane Storage System Derived From Corncobs Citat: "...Pfeifer and his colleagues at MU and MRI discovered that that fractal pore spaces [i majskolber] (spaces created by repetition of similar patterns at different scales) are remarkably efficient at storing natural gas..."
Eksterne henvisninger
- Metanudslip fra tundraen
- Methane hydrate ice: A Possible Mechanism For Ice Age And Global Warming Cycles Citat: "...Current Estimates of Methane Hydrates are on the order of 1 to 2 Million Trillion Cubic Feet..."
- Methane ice worms: Hesiocaeca methanicola colonizing fossil fuel reserves
- Stor flod af metan og ethan fundet på Saturns måne Titan. Videnskab.dk 2012 Arkiveret 15. august 2017 hos Wayback Machine
- Forskere: Sådan kan liv i rummet eksistere uden vand. Videnskab.dk
Medier brugt på denne side
Structure of methane
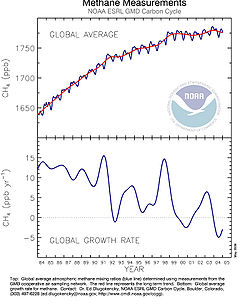
Atmospheric Methane measurements 1984-2005
Top: Global average methane mixing ratios from the GMD cooperative air sampling network.
Bottom: Global average growth rate for methane.Two computer models showing the amount of methane found at the Earth's surface and in the stratosphere.