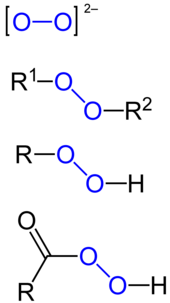
Peroxid
Et peroxid er en kemisk forbindelse, der indeholder to sammenhængende oxygenatomer. Forbindelsen dannes ved en reaktion med ilt. Der findes både organiske og uorganiske peroxider.
De fleste peroxider er meget reaktive og stærkt oxiderende, og særligt de organiske peroxider er eksplosions- og brandfarlige.
Det enkleste peroxid er brintoverilte, der er relativt ufarlig og anvendes som blegemiddel samt til desinfektion.
Se også
|
Medier brugt på denne side
Peroxide_group