Natriumthiosulfat
| Natriumthiosulfat | |
|---|---|
 | |
| IUPAC-navn Natriumthiosulfat | |
| Generelt | |
| Andre navne | Natriumhyposulfit, fiksersalt, antiklor |
| Molekylformel | Na2S2O3 |
| Molarmasse | 158,108 g/mol |
| Fremtræden | Hvide krystaller |
| CAS-nummer | |
| PubChem | |
| Kemiske egenskaber | |
| Massefylde | 1,667 g/cm3 |
| Opløselighed i vand | 20,9 g/100 ml (20 °C) |
| Smeltepunkt | 48,3 °C (pentahydrat) |
| Kogepunkt | 100 °C (pentahydrat, -5H2O) |
| Sikkerhed | |
| MSDS | MSDS (Sikkerhedsdatablad) |
| EU klassifikation | ikke listet |
| NFPA 704 | |
| Flammepunkt | Ikke-brændbar |
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |
Natriumthiosulfat er et thiosulfatsalt af natrium med sumformel: Na2S2O3. Med fem krystalvand, Na2S2O3•5H2O, kendes forbindelsen under navnene fiksersalt og antiklor.
Karakterisk reaktion og brug
En karakterisk reaktion for thiosulfatanionen er reaktionen med fortyndet syrer hvorved dannes svovl, svovldioxid og vand:[1]
Denne reaktion kendes under navnet clock reaktionen idet når svovlkoncentrationen når et vist niveau skifter farven fra farveløs til svagt gul. Reaktionen har været brugt til at danne kolloidt svolv. Hvis reaktionen udføres ved lav temperatur opnås thiosvovlsyre (H2S2O3), som er en stærk syre med pKa på 0,6 og 1,7 for første og anden syrestyrkekonstant.
Guld ekstraktion
Natriumthiosulfat benyttes som alternativt reagens i stedet for cyanid ved ekstraktion af guld.[2] Det danner et stærkt kompleks med guld(I)-ioner, [Au(S2O3)2]3-. Fordelen med denne metode er at thiosulfat er essentielt ugiftig. Ulempen er at den kræver et stort forbrug af thiosulfat pga. manglende genbrugsteknikker. I modsætning til [[Au(S2O3)2]]3-, absorberes thiosulfatkomplekset ikke på aktivt kul, som er standardteknikken når cyanid benyttes.
Analytisk kemi
Natriumthiosulfat benyttes også i analytisk kemi. Når thiosulfat opvarmes med en prøve der indeholder "aluminiumkationer" udfældes et hvidt produkt:
Reference
| Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
Medier brugt på denne side
Chemistry, Chemical Template
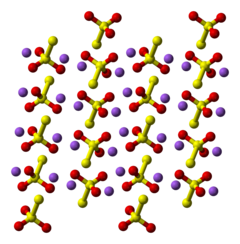
Ball-and-stick model of part of the crystal structure of anhydrous sodium thiosufate, Na2[S2O3].
X-ray crystallographic data from Acta Cryst. (1961). 14, 237-243.
Model constructed in CrystalMaker 8.1.
Image generated in Accelrys DS Visualizer.




