Natriumhydroxid
Der er ingen kildehenvisninger i denne artikel, hvilket er et problem. (marts 2020) (Lær hvordan og hvornår man kan fjerne denne skabelonbesked) |
Natriumhydroxid | |
|---|---|
| Synonymer | Kaustisk soda, afløbsrens |
| Struktur |  |
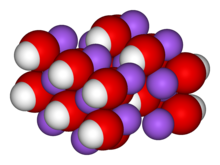
| Kuglekalot-model |  |
| Sumformel | NaOH |
| Farve | Farveløs |
Fysiske egenskaber | |
| Molvægt | 40 g/mol |
| Smeltepunkt | 323 °C |
| Kogepunkt | 1388 °C |
| Massefylde | 2.13 g/cm3 (stuetemp.) |
| Varmefylde | 1,5 kJ/(kg*K) |
Syre/base-egenskaber | |
| pKa | 15,7 |
Diverse | |
| CAS-nummer | 1310-73-2 |
| E-nummer | |

Natriumhydroxid (NaOH) er en stærk base. Den består af ionerne Na+ og OH-.[1]
Anvendelse
Natriumhydroxid kan bl.a. bruges til at rense tilstoppede afløb (opløse hår og fedt), fremstille sæbe og til at afsyre træ. Natriumhydroxid har forskellige handelsnavne som f.eks. kaustisk soda, ætsnatron og natronlud.
Man kan ved brug af kaustisk soda i pulverform, kogende vand og en håndfuld forzinkede søm give kobbermønter som 25-ører og 50-ører en overflade og farve, der minder om sølv.
Anvendes i produktionen af biodiesel.
Sikkerhed
Natriumhydroxid er stærkt ætsende på hud, slimhinder og andet væv på mennesker og dyr samt på mange tekstiler. Det forårsager hurtigt dybe ætseskader ved hudkontakt og er blandt de farligste kemikalier som forekommer i hjemmet. At anvende natriumhydroxid til at opløse propper i afløbet er meget farligt, da indånding af støv fra pulveret eller det mindste stænk på hud, tøj eller øjne giver alvorlige ætseskader. Indtagelse er livsfarligt.
Ved kontakt med natriumhydroxid, følg anvisningerne på flasken.
Kilder
| Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
|
Medier brugt på denne side
Chemistry, Chemical Template
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Forfatter/Opretter: Claudio Pistilli, Licens: CC BY-SA 4.0
Sodium hydroxide 3D chemical structure





