Mitokondrie


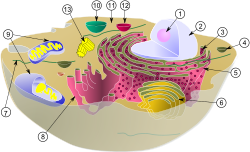
1. Nukleolus
2. Nukleus
3. Ribosomer (små prikker)
4. Vesikel
5. Granulært (ru) endoplasmatisk reticulum
6. Golgiapparattet
7. Cytoskelet
8. Glat endoplasmatisk reticulum
9. Mitokondrier
10. Vakuole
11. Cytosol
12. Lysosom
13. Centrioler
Et mitokondrie (af græsk μίτος mitos, ”tråd”, og χονδρίον chondrion, diminutiv af chondros, ”korn”) er inden for cellebiologi betegnelsen for et organel, som findes i de fleste eukaryote celler. Et mitokondrie måler mellem 0,5 og 1,0 mikrometer (μm) i diameter. Mitokondrier kaldes ofte ”cellens kraftværker”, fordi de producerer hovedparten af cellens adenosintrifosfat (ATP), der rummer kemisk energi. Ud over energiproduktion er mitokondrier involveret i en række andre processer såsom cellesignalering, celledeling og apoptose (programmeret celledød), og de medvirker desuden ved overvågningen af cellens cyklus og vækst. Mitokondrier er også knyttet til visse sygdomme – herunder mitokondriesygdomme og hjertedysfunktion – og menes at spille en rolle i aldringsprocessen.
Antallet af mitokondrier i en celle varierer afhængigt af organisme- og vævstype. Nogle celler indeholder kun ét mitokondrie, men de fleste indeholder flere tusinde mitokondrier. Røde blodlegmer indeholder ingen mitokrondrier. Mitokondriet er opdelt i specialiserede funktionelle områder. Disse områder omfatter ydermembranen, det intermembranøse rum, indermembranen, cristae og matrix. Mitokondrielle proteiner varierer alt efter væv og art. Hos mennesket er der blevet identificeret 615 typer af proteiner i hjertets mitokondrier,[1] og i rotters mitokondrier er der blevet fundet 940 proteiner.[2] Mitokondrier har også deres eget genom, som har vist sig at minde om bakteriers genomer.
Historie
De første observationer af mitokondrielignende intracellulære strukturer blev offentliggjort i 1840'erne.[3] Richard Altmann identificerede dem som organeller og kaldte dem "bioblaster".[3] I 1898 gav Carl Benda dem navnet 'mitokondrier'.[3] I 1904 opdagede Friedrich Meves mitokondrier i planter (i åkander).[3][4] Som den første satte B.F. Kingsbury dem i 1912 i forbindelse med cellerespiration, dog kun på baggrund af morfologiske undersøgelser.[3] Philip Siekevitz kaldte dem i 1957 for "cellens kraftværker".[5]
Struktur
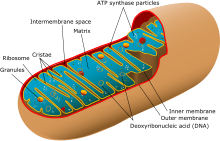
Mitokondrier er omsluttet af en ydre og indre membran, der begge består af et dobbeltlag af fosfolipider og proteiner.[6] De to membraner har forskellige egenskaber. På grund af de to membraner kan mitokondriet opdeles i fem områder:
- Ydermembranen
- Det intermembranøse rum (mellemrummet mellem yder- og indermembranen)
- Indermembranen
- Cristae (fingerlignende indfoldninger i indermembranen)
- Matrix (området inden for indermembranen)
Ydermembranen
Mitokondriets ydermembran, der omslutter hele mitokondriet, har et protein/fosfolipid-forhold svarende til en eukaryot celles plasmamembran (cirka 1:1 målt på vægt). I ydermembranen er der indlejret poriner (en type kanalprotein), der tillader molekyler på op til 5000 Dalton at diffundere fra den ene til den anden side af ydermembranen.[6] Store proteiner transporteres gennem membranen af proteinkomplekser kaldt TOM (translocase of the outer membrane): En signalsekvens for enden af proteinets N-terminus mødes med en receptor på komplekset, hvilket igangsætter aktiv transport.[7] Beskadigelse af ydermembranen kan medføre, at proteiner i det intermembranøse rum lækker ud i cytosolen og slår cellen ihjel.[8] Ydermembranen kan fusionere med membranen i det endoplasmatiske reticulum (ER) i en særlig struktur ved navn MAM (mitokondrie-associeret ER-membran). Dette er vigtigt for calciumsignaleringen mellem ER og mitokondrierne og udvekslingen af lipider mellem ER og mitokondrier.[9]
Det intermembranøse rum
Det intermembranøse rum er mellemrummet mellem yder- og indermembranen. Det kaldes også det perimitokondrielle rum. Fordi den ydre membran er gennemtrængelig for små molekyler, er koncentrationen af små molekyler (f.eks. ioner og kulhydrater) den samme som i cytosolen.[6] Proteiner, der er store molekyler, må dog have en specifik signalsekvens for at blive transporteret gennem ydermembranen, så proteinsammensætningen i det intermembranøse rum er forskellig fra den i cytosolen. Et protein, der findes i det intermembranøse rum, men ikke i cytosolen, er cytokrom C.[8]
Indermembranen
Indermembranen indeholder proteiner med fem typer funktioner:[6]
- Enzymer, der udfører redoxreaktioner i forbindelse med oxidativ fosforylering
- ATP-syntase, som danner adenosintrifosfat (ATP) i matrix
- Specifikke transportproteiner, der regulerer passagen af nærings- og affaldsstoffer ind og ud af matrix
- Proteinimportører
- Mitokondrielle fusions- og fissionsproteiner
Indermembranen indeholder mere end 151 forskellige polypeptider og har et meget højt protein/fosfolipid-forhold (mere end 3:1 målt på vægt svarende til 15 fosfolipider pr. protein). Indermembranen rummer cirka 1/5 af den samlede proteinmængde i et mitokondrie.[6] Derudover er indermembranen rig på et usædvanligt fosfolipid: Cardiolipin. Dette fosfolipid blev oprindeligt fundet i hjerter fra tamkvæg i 1942 og er karakteristisk for mitokondriers membraner og bakteriers plasmamembraner.[10] Cardiolipin er et "dobbelt" fosfolipid og indeholder derfor to fosfatgrupper samt fire fedtsyrer, og er med til at gøre indermembranen uigennemtrængelig.[6] I modsætning til ydermembranen er der ikke indlejret poriner i indermembranen, hvilket øger dens uigennemtrængelighed for alle slags molekyler. Stort set alle ioner og molekyler behøver derfor hjælp fra specielle transportproteiner for at passere denne membran. Proteiner transporteres ind i matrix via proteinkomplekset TIM (translocase of the inner membrane) eller via komplekset Oxa1.[7] Desuden er der et membranpotential over indermembranen, som skyldes enzymers udpumpning af hydrogenioner (H+) fra matrix som led i elektrontransportkæden.
Cristae

Indermembranen danner talrige folder kaldt cristae, som udvider indermembranens overfladeareal, hvilket styrker dens evne til at producere ATP. For et typisk levermitokondrie er arealet af indermembranen omtrent fem gange så stor som ydermembranens areal. Forholdet varierer dog, og i celler med større behov for ATP kan mitokondrierne have flere cristae. Folderne er besat med små runde legemer kendt som F1-partikler eller oxysomer. Disse legemer er små invaginationer af indermembranen med betydning for den kemiosmotiske funktion.[11]
Et nyligt studium inden for matematisk modellering peger på, at cristae’ne i filamentøse mitokondrier på grund af deres optiske egenskaber kan påvirke udviklingen og udbredelsen af lys i væv.[12]
Matrix
Matrixen er mitokondriets inderområde, der er omsluttet af indermembranen. Den indeholder omkring 2/3 af alt protein i et mitokondrie.[6] Matrixen spiller sammen med indermembranens ATP-syntase en central rolle i syntesen af ATP. Matrixen er rig på enzymer (den indeholder flere hundrede forskellige slags) og indeholder desuden mitokondrielle ribosomer, tRNA og kopier af mitokondriets eget DNA-molekyle. Enzymernes hovedopgaver er oxidation af pyruvat og fedtsyrer samt opgaver i forbindelse med citronsyrecyklussen.[6]
Som nævnt har mitokondrier deres eget arvemateriale (DNA), og de har også det nødvendige maskineri til syntese af RNA og proteiner (læs også: proteinsyntese). Der er blevet fundet 16.569 basepar i humant mtDNA. Disse koder for 37 gener: 22 for tRNA, 2 for rRNA og 13 for peptider.[13] De 13 mitokondrielle peptider er indbygget i indermembranen. Andre proteiner, hvis opbygning er indkodet i cellekernens DNA, er også indbygget i indermembranen.
Mitokondrie-associeret ER-membran
Den mitokondrie-associerede ER-membran (MAM) er en struktur, der spiller en væsentlig rolle for cellens fysiologi og homøostase. Med elektronmikroskopi blev det opdaget, at mitokondriets ydermembran kan binde sig til membranen i ER, og dette er blevet bekræftet ved hjælp af fluorescensmikroskopi.[14] Undersøgelser har vist, at afstanden mellem mitokondrierne og ER blot er 10-25 nm ved MAM, og at de to membraner holdes sammen af komplekser af bindingsproteiner.[9][14][15]
Oprenset MAM fra subcellulær fraktionering har vist sig at være rig på enzymer involveret i udvekslingen af fosfolipider samt kanaler til calciumsignalering.[14][15] Dette tyder på, at mitokondrier spiller en vigtig rolle i oplagringen af lipider og ved signaltransduktion.
Transport af fosfolipider
MAM er rig på enzymer involveret i lipid-biosyntesen såsom fosfatidylserin-syntase på ER-siden og fosfatidylserin-decarboxylase på mitokondriesiden.[16][17] Fordi mitokondrier er dynamiske organeller, der konstant deler sig eller fusionerer med hinanden, har de brug for en vedvarende og velreguleret forsyning af fosfolipider for at holde deres membraner ved lige.[18][19] Mitokondrier er dog ikke kun opsamlingssted for de fosfolipider, hvis syntese de færdiggør; mitokondrier virker også som mellemstation for færdige og halvfærdige fosfolipider og medvirker desuden ved ceramid- og kolesterolmetabolismen og glykosfingolipid-anabolismen.[17][19]
Denne intracellulære trafik afhænger af MAM, der har vist sig at formidle transporten af halvfærdige lipider imellem organeller.[16] Mens lipider normalt transporteres i vesikler, tillader den korte afstand mellem ER og mitokondriets ydermembran, at de ”springer” fra den ene membran til den anden.[19] Forunderligt nok kræver denne usædvanlige og tilsyneladende besværlige mekanisme ikke energi fra ATP.[19] Mekanismen har tværtimod vist sig at være afhængig af særlige proteinkomplekser kaldt ERMES (ER-mitochondria encounter structure). Det er dog endnu usikkert, om dette kompleks direkte hjælper lipiderne med at springe fra membran til membran eller blot holder membranerne tilstrækkeligt tæt sammen, til at lipiderne kan springe uden at forbruge energi.[19][20]
MAM ser også ud til at fungere som mellemstation mellem ER og Golgiapparatet i den proces, der fører til dannelse og sekretion af very-low-density lipoprotein (VLDL).[17][21]
Calciumsignalering
MAM hjælper også ER og mitokondrierne med at udveksle calciumioner. Udvekslingen foregår via komplekser af glykoproteinet IP3R, der fungerer som Ca2+-kanal i ER-membranen.[9][14] På MAM findes også calciumreceptoren VDAC1, der tillader frie calciumioner i cytosolen at trænge ind i mitokondrierne. Mitokondriers evne til at fungere som afløb for Ca2+ skyldes den elektrokemiske gradient, som er opbygget ved oxidativ fosforylering, og som gør transporten af Ca2+ til en exergon (ikke-energikrævende) proces.[22]
Organisering og forekomst
Mitokondrier findes i næsten alle eukaryoter.[23] De varierer i antal og placering alt efter celletype. Encellede organismer indeholder ofte ét enkelt mitokondrie. I menneskets leverceller findes der derimod mellem 1000 og 2000 mitokondrier i hver celle, hvor de udgør op til 1/5 af cellens volumen.[6] Mitokondrier findes imellem myofibriller i muskler og omkring sædcellers flagel.[6] De danner ofte et komplekst tredimensionalt netværk med værtscellens cytoskelet. Cytoskelettet bestemmer mitokondriernes form og kan således påvirke deres funktion.[24] Det er sandsynligt, at det intermediære filament vimentin, der findes i cytoskelettet, har betydning for mitokondriernes binding til cytoskelettet.[25]
Røde blodlegemer og terminale keratinocytter (i hudens yderste lag) har ikke mitokondrier. Røde blodlegemer danner ATP udelukkende ved glykolyse.[26]
Funktion
Mitokondriernes hovedfunktion er at producere adenosintrifosfat (ATP), der forsyner cellen med energi.[27][28] ATP afgiver energi ved omdannelse til adenosindifosfat og uorganisk fosfat (Pi), og denne reaktion kan derfor drive energikrævende (endergone) reaktioner i cellen. Ud over ATP-produktion tjener mitokondrierne en række andre formål. Energien bundet i ATP stammer fortrinsvis fra oxidation (forbrænding) af pyruvat, selvom mitokondrier også kan oxidere lipider.
Energiomdannelse
Mitokondriets indermembran indeholder et stort antal proteiner, der medvirker til produktionen af ATP. Første skridt i dannelsen af ATP er oxidationen af pyruvat, som er blevet dannet af glukose i cellens cytosol.[29] Oxidationen af pyruvat, kendt som cellulær respiration, kræver tilstedeværelse af ilt. Har cellen ikke adgang til ilt, nedbrydes cellens glukose ved anaerob fermentering. Denne proces foregår uafhængigt af mitokondrierne.[30] Produktionen af ATP ved nedbrydning af glukose via aerob respiration er cirka 13 gange så effektiv som ved fermentering.[31] Det er for nylig blevet opdaget, at planters mitokondrier kan producere små mængder ATP uden ilt ved i stedet at bruge nitrit.[32]
Pyruvat og citronsyrecyklussen
Hvert pyruvat-molekyle, som dannes ved glykolyse i cytosolen, transporteres ved aktiv transport gennem mitokondriets indermembran til matrix, hvor det oxideres og bindes til coenzym A under dannelse af CO2, acetyl-coenzym A (acetyl-CoA) og NADH.[30]
Acetyl-CoA oxideres videre af enzymer, der hører til citronsyrecyklussen (Krebs’ cyklus). Disse enzymer findes i matrix med undtagelse af succinat-dehydrogenase, som er bundet til indermembranen som en del af respiratorisk kompleks II.[33] I citronsyrecyklussen oxideres (forbrændes) acetyl-CoA via mange mellemled til CO2. Ved denne proces dannes reducerede cofaktorer (tre molekyler NADH og ét molekyle FADH2 for hvert molekyle acetyl-CoA). Disse cofaktorer tjener som elektronkilder for elektrontransportkæden. Ved processen dannes også et molekyle GTP (som let omdannes til ATP).[30]
NADH og FADH2: elektrontransportkæden

Energien fra NADH og FADH2 overføres trinvist til ilt (O2) via elektrontransportkæden. NADH og FADH2 dannes i matrix via citronsyrecyklussen, men dannes også i cytoplasmaet ved glykolyse. (NADH dannet i cytoplasma kan som NAD+ (oxideret form) transporteres ind i mitokondriets matrix ved hjælp af malat og en antiporter. Inde i matrix reduceres NAD+ tilbage til NADH). Proteinkomplekser i indermembranen (NADH-dehydrogenase, cytokrom-C-reduktase og cytokrom-C-oxidase) varetager overførslen af elektroner til ilt, og energien, som herved frigøres, bruges til at pumpe hydrogenioner (H+) ud i det intermembranøse rum. Det hænder, at elektroner binder til ilt for tidligt, så der opstår reaktive iltradikaler som f.eks. superoxid (O2-).[30] Dette kan forårsage oxidativ stress i mitokondriet og skade dets funktion, hvilket menes at være årsag til aldringsprocessen.[34]
Når koncentrationen af hydrogenioner i det intermembranøse rum øges, opbygges en stærk elektrokemisk gradient over indermembranen. Hydrogenionerne kan vende tilbage til matrix via ATP-syntase-komplekset, hvorved deres energi bruges til at syntetisere ATP ud fra ADP og uorganisk fosfat (Pi).[30] Processen kaldes kemiosmose og blev første gang beskrevet af Peter D. Mitchell,[35][36] der i 1978 modtog nobelprisen i kemi for sit arbejde. I 1997 blev en del af nobelprisen i kemi givet til Paul D. Boyer og John E. Walker for deres opklaring af ATP-syntases virkemåde (den tredje modtager var danske Jens C. Skou for opdagelsen af natrium-kalium-pumpen).[37]
Varmeproduktion
Under visse forhold kan hydrogenionerne vende tilbage til mitokondriets matrix uden at bidrage til ATP-syntesen. Denne proces kaldes hydrogenion-lækage og skyldes hydrogenionernes faciliterede diffusion ind i matrix. Den potentielle energi, som findes i den elektrokemiske energi, omdannes til varme i stedet for at bindes i ATP. Processen varetages af en H+-kanal kaldt thermogenin eller UCP1.[38] Thermogenin er et protein på 33.000 Da, der blev opdaget i 1973.[39] Thermogenin findes primært i brunt fedtvæv. Brunt fedtvæv findes hos pattedyr og optræder i størst mængde tidligt i livet og hos dyr i dvale. Hos mennesker er mængden af brunt fedtvæv størst ved fødslen, hvorefter mængden svinder ind med alderen.[38]
Lagring af calciumioner

Mængden af frie calciumioner (Ca2+) i cellen kan regulere en række reaktioner og er vigtig for signaltransduktion i cellen. Mitokondrier kan lagre calciumioner kortvarigt og hjælper således med at opretholde cellens calciumbalance.[40] Deres evne til hurtigt at optage calcium til senere frigivelse gør dem til gode ”cytosoliske buffere” for calcium.[41][42][43] Det endoplasmatiske reticulum (ER) er det væsentligste calciumdepot i cellen, og der hersker et betydeligt samspil mellem mitokondrier og ER med hensyn til lagring af calcium.[44] Calciumionerne transporteres passivt gennem mitokondriernes indermembran til matrix af en calcium-uniporter. Transporten drives hovedsageligt af mitokondriernes membranpotential,[40] der skyldes mængden af elektroner på indersiden og hydrogenioner (H+) på ydersiden af indermembranen. Transport af calcium-ioner ud af mitokondrierne kan foregå via en natrium-calcium-antiporter eller via ”calcium-induceret calciumfrigivelse”.[45] Frigivelse af calciumioner kan ændre cellens membranpotential drastisk. Dette kan aktivere en række sekundære budbringerproteiner, som kan igangsætte processer som frigivelse af neurotransmitter i nerveceller eller hormoner i kirtelceller.
Øvrige funktioner
Mitokondrier spiller en central rolle i mange andre opgaver, herunder:
- Regulation af membranpotential[30]
- Apoptose (programmeret celledød)[46]
- Calciumsignalering (herunder calcium-initieret apoptose)[47]
- Regulation af cellens stofskifte[48]
- Visse reaktioner i hæm-syntesen[49]
- Steroidsyntese[41]
Visse mitokondrielle funktioner udføres kun i specifikke celletyper. Eksempelvis indeholder mitokondrierne i leverceller enzymer, der gør dem i stand til at afgifte ammoniak, der dannes som affaldsprodukt ved forbrænding af proteiner. En mutation i et af generne, der regulerer en af disse funktioner, kan resultere i mitokondriesygdomme.
Regulering af celledeling
Mitokondriers indflydelse på celledeling er blevet undersøgt ved hjælp af HeLa-celler (livmoderhalskræftceller). Tumorceller kræver en rigelig forsyning af adenosintrifosfat (ATP) for at syntetisere bioaktive molekyler som lipider, proteiner og nukleotider, der er nødvendige for hurtig celledeling.[50] Hovedparten af ATP’en i tumorceller dannes ved oxidativ fosforylering.[51] Forstyrrelse af denne mekanisme har vist sig at standse cellen i dens cyklus, hvilket tyder på, at mitokondrier spiller en rolle ved celledeling. Mitokondriel ATP er også vital for regulering af cellevolumen, koncentration af opløste stoffer samt cellestruktur.[52][53][54] ATP-niveauet varierer afhængigt af fase i cellecyklussen, så tilsyneladende er der en sammenhæng mellem ATP-mængden og cellens evne til at genindtræde i cyklussen.[55] Selvom de specifikke mekanismer endnu ikke er kendte, tyder studier på, at kontrolpunkter imellem faser i cellecyklussen kontrollerer mængden af tilgængelig energi, før cyklussen får lov at fortsætte.[48]
Oprindelse
Mitokondrier har meget til fælles med prokaryoter. Af den grund menes de at nedstamme fra endosymbiotiske prokaryoter.
Et mitokondrie indeholder DNA, der er organiseret som kopier af det samme cirkulære kromosom. Dette mitokondrielle kromosom rummer gener for bl.a. de redox-enzymer, der indgår i respirationskæden. Det mitokondrielle genom koder for rRNA og 22 tRNA-molekyler, som er nødvendige for translation af mRNA til protein. Den cirkulære DNA-struktur findes også hos prokaryoter; desuden minder mitokondriets genetiske kode, der afviger en anelse fra den universelle genetiske kode, om proteobakteriernes genom.[56] Disse forhold underbygger, at forløberen for mitokondriet, det såkaldte protomitokondrie, tilhørte proteobakteriernes række.[56] Mere præcist menes protomitokondriet at have været nært beslægtet med rickettsierne (en gruppe prokaryote parasitter).[57] Det præcise slægtskab mellem mitokondriets forløber og alfa-proteobakterierne samt spørgsmålet om, hvorvidt mitokondriet opstod samtidig med eller senere end cellekernen, står dog fortsat hen i det uvisse.[58]
Et nyligt studium foretaget af forskere ved University of Hawai’i at Mānoa og Oregon State University tyder på, at SAR11-bakterierne (Pelagibacteraceae), der forekommer i meget stort antal i havet, og mitokondrierne i de fleste eukaryote celler har en fælles ”stamfar”.[59]
Ribosomerne, som det mitokondrielle DNA koder for, minder om bakterielle ribosomer med hensyn til størrelse og struktur.[60] De ligner det bakterielle 70S-ribosom og ikke de cytoplasmatiske 80S-ribosomer, som dannes af nukleolus i cellekernen.
Det endosymbiotiske forhold mellem mitokondrier og deres værtsceller blev populariseret af Lynn Margulis.[61] Ifølge den såkaldte endosymbiontteori udviklede mitokondrierne sig fra bakterier, der på en eller anden måde overlevede at blive endocyteret af en anden celle og siden blev en del af dennes cytoplasma. Bakteriernes evne til at udføre respiration i værtscellerne, der tidligere havde fået al deres energi fra glykolyse og fermentering, gav disse værtsceller en betydelig evolutionær fordel. På samme måde fik værtsceller i symbiose med bakterier, der var i stand til at udføre fotosyntese, en fordel. Denne symbiose udvidede det område, som værtscellerne kunne leve i, ganske betydeligt. Det symbiotiske forhold opstod sandsynligvis for mellem 1,7[62] og 2[63] milliarder år siden.
Nogle få grupper af encellede eukaryoter har ikke mitokondrier: mikrosporidierne, metamonader og archamoebae.[64] Disse grupper fremgår som de mest primitive eukaryoter, når de vises på fylogenetiske træer lavet ved hjælp af rRNA-information, hvilket kunne tyde på, at de opstod før mitokondrierne. Dette er dog ikke rigtigt: De er i virkeligheden afledte grupper af mitokondrier og rummer gener og organeller fra mitokondrier (f.eks. mitosomer og hydrogenosomer).[23]
Genom

Mitokondrier har selvstændige arveanlæg (DNA), og det skyldes formentlig, at de har været selvstændige, bakterieagtige organismer engang.[65] Mitokondrie-DNA'et bliver kun videreført af moren. Farens mitokondrie-DNA går så at sige til grunde, når han selv dør. Heraf taler nogen om den mitokondrielle Eva.
Menneskets mitokondrielle genom består af et cirkulært DNA-molekyle med 16.569 basepar.[13][66] Det mitokondrielle genom koder for 37 gener: 13 for subunits i de respiratoriske komplekser I, III, IV og V, 22 for mitokondriel tRNA (for de 20 almindelige aminosyrer samt en ekstra for hver af de to aminosyrer leucin og serin) samt 2 for rRNA.[66] Hvert mitokondrie kan indeholde 2-10 kopier af sit DNA.[67]
Ligesom for prokaryoter er der en stor andel af kodende DNA og ingen gentagelsessekvenser. Mitokondrielle gener transskriberes til multigene transskripter, som kløves og polyadenyleres for at blive til modne transskripter. Mitokondrielt DNA koder kun for ca. 5 % af de proteiner, der er nødvendige for mitokondriets funktion;[68] det er generne i cellekernen, der koder for de fleste, og disse proteiner må transporteres ind i mitokondriet.[13] Det præcise antal gener indkodet i henholdsvis cellekernen og det mitokondrielle DNA varierer med arten. Det mitokondrielle genom er generelt cirkulært, men undtagelser er kendt.[69] Generelt mangler mtDNA introns, hvilket er tilfældet for det humane mitokondrielle genom;[13] der er dog blevet fundet introns i visse eukaryoters mtDNA,[70] f.eks. hos gær[71] og protister,[72] herunder Dictyostelium discoideum.[73]
Hos dyr består det mitokondrielle genom af ét enkelt cirkulært kromosom, der er omtrent 16.000 basepar langt og indeholder 37 gener. Genernes placering kan variere. Den cirkulære struktur ses dog ikke hos menneskelusen (Pediculus humanus). I stedet er deres mitokondrielle genom fordelt på 18 små cirkulære kromosomer, der hver er 3-4 tusind basepar lange og har mellem 1 og 3 gener.[74] Dette mønster ses også hos andre sugende lus, men ikke hos bidende lus. Det har vist sig, at der mellem de små kromosomer kan ske rekombination.
Mitokondriers genetiske kode afviger en anelse fra den universelle genetiske kode. Dette blev forudsagt allerede i 1973,[75] men først bevist i 1979, da forskere, der undersøgte generne i menneskets mitokondrier, slog fast, at generne benyttede sig af en alternativ kode.[76] Siden er der blevet opdaget forskellige varianter af denne alternative mitokondrielle kode.[77][78] Hos mitokondrier er de tre codons AUA, AUC og AUU tilladte start-codons.
| Organisme | Codon | Standard | Mitokondrier |
|---|---|---|---|
| Pattedyr | AGA, AGG | Arginin | Stop |
| Hvirvelløse dyr | AGA, AGG | Arginin | Serin |
| Svampe | CUA | Leucin | Threonin |
| Alle de ovenstående | AUA | Isoleucin | Methionin |
| UGA | Stop | Tryptofan |
Nogle af disse forskelle skyldes RNA-redigering (ændring af RNA-sekvensen ved f.eks. tilføjelse eller konvertering af nukleosider), som er almindeligt for mitokondrier. Tidligere troede man, at CGG i højerestående planter kodede for tryptofan i stedet for arginin; det blev dog opdaget, at codonet i den editerede RNA-sekvens var UGG, der svarer til den universelle genetiske kode for tryptofan.[79] Bemærkelsesværdigt er det, at den mitokondrielle genetiske kode hos leddyr har undergået en parallel evolution inden for samme række, således at nogle organismer translaterer AGG til aminosyren lysin.[80]
Mitokondrielle genomer har langt færre gener end de bakterier, som mitokondrier menes at nedstamme fra. Nogle er helt gået tabt, og mange er blevet overført til cellekernen, eksempelvis dem, der koder for underenhederne i respiratorisk proteinkompleks II.[66] Nogle få organismer, f.eks. Cryptosporidium, har mitokondrier, der fuldstændig mangler DNA, muligvis fordi alle deres gener er gået tabt eller er blevet overført.[81] Hos Cryptosporidium har mitokondrierne et anderledes ATP-syntese-apparat, der gør parasitten resistent over for almindelige mitokondrie-inhibitorer såsom cyanid, azid og atovaquon.
Formering og nedarvning
Mitokondrier deler sig ved binær fission, der minder om bakteriers formering;[68] i modsætning til bakterier er mitokondrier dog også i stand til at fusionere med andre mitokondrier.[66][82] Reguleringen af mitokondriers deling varierer fra eukaryot til eukaryot. Hos mange encellede eukaryoter er mitokondriernes vækst knyttet til cellecyklussen. Et mitokondrie kan eksempelvis dele sig synkront med cellekernen. Delings- og adskillelsesprocessen må kontrolleres nøje, således at hver dattercelle får mindst ét mitokondrie. Hos andre eukaryoter (f.eks. pattedyr) deler mitokondrierne sig hovedsageligt som respons på værtscellens energibehov og i mindre grad som led i cellecyklussen. Når en celles energibehov er stort, vil mitokondrierne vokse og dele sig. Når energibehovet derimod er lille, nedbrydes eller inaktiveres mitokondrierne. Hos flercellede eukaryoter fordeles mitokondrierne tilsyneladende tilfældigt i de to datterceller, når en celle deler sig (i modsætning til hos encellede eukaryoter). Undersøgelse af mitokondriers dynamik, det vil sige forholdet mellem mitokondriers fusion og fission, har vist, at funktionelle og strukturelle ændringer i mitokondriers morfologi spiller en vigtig rolle ved mange sygdomme.[83]
Et individs mitokondrielle gener nedarves ikke på samme måde som generne i cellekernen. Typisk nedarves mitokondrierne kun fra den ene af forældrene. Når en menneskelig ægcelle bliver befrugtet af en sædcelle, bidrager æggets og sædens cellekerner ligeligt til zygotens DNA. Derimod stammer mitokondrierne og dermed også det mitokondrielle DNA fra ægcellen alene. Sædcellens mitokondrier trænger ind i ægcellen, men bidrager ikke med genetisk information til embryoet.[84] Tværtimod mærkes de paternelle mitokondrier med signalstoffet ubiquitin, der gør, at de senere nedbrydes i embryoet.[85] Ægcellen indeholder relativt få mitokondrier, men det er udelukkende disse, som overlever og deler sig for at forsyne organismens celler med mitokondrier. Af den grund nedarves mitokondrier næsten udelukkende maternelt (fra moren). Dette fænomen ses hos de fleste organismer, heriblandt samtlige dyrearter. Hos nogle arter kan mitokondrierne dog nedarves paternelt (fra faren). Dette er normalt hos visse nåle- og takstræer.[86] Det menes at ske ganske sjældent hos mennesker.[87] Ifølge en nylig teori forbliver mitokondrier, der forkorter mænds levetid, i systemet, fordi mitokondrier kun nedarves fra moren. Mitokondrier, der forkorter kvinders levetid, vil derimod sjældnere nå at blive videreført til næste generation, således at disse mitokondrier ”vælges fra” ved naturlig selektion. Af den grund menes kvinder og dyr af hunkøn at leve længere end individer af det modsatte køn. Forfatterne bag teorien hævder, at dette er en delvis forklaring.[88]
Det forhold, at mitokondrier nedarves fra den ene af forældrene, nedsætter sandsynligheden for genetisk rekombination mellem forskellige linjer af mitokondrier, selvom et enkelt mitokondrie kan indeholde 2-10 kopier af sit DNA. Derfor menes mitokondrier at dele sig ved binær fission. Visse studier tyder dog på, at der kan ske rekombination i mtDNA. Enzymerne, der er nødvendige for rekombination, findes i pattedyrsceller.[89] Desuden er der tegn på, at mitokondrier hos dyr kan undergå rekombination.[90] For mennesker er dataene mere usikre, men der er indirekte beviser for, at rekombination forekommer.[91][92] Hvis der ikke forekommer rekombination, udgør hele mtDNA-sekvensen et enkelt haplotype, som gør det nyttigt i studiet af en populations evolutionære historie.
Evolutionære studier
Fordi der stort set ikke dannes nye genkombinationer i mitokondriets DNA, er mtDNA et nyttigt værktøj i populationsgenetik og evolutionsbiologi.[93] Idet al mtDNA nedarves som en enkelt enhed (haplotype), kan videreførelsen af mtDNA fra individ til individ illustreres som et genetisk træ. Et sådant træ kan bruges til at udlede en befolknings evolutionære historie. Det klassiske eksempel er udforskningen af menneskets udvikling, og man taler om den mitokondrielle Eva, der tænkes at være ophav til alle nulevende menneskers mtDNA. Ved at undersøge og sammenligne mutationer i mtDNA fra fossiler (en metode kendt som det molekylære ur) er det muligt at finde ud af, hvornår den mitokondrielle Eva levede, og hvornår mennesket således blev en selvstændig art.[94][95] Et andet eksempel er sekventeringen af mtDNA fra knogler af neandertalere. Den relativt store forskel på mtDNA-sekvensen hos neandertalere og moderne mennesker tolkes som et bevis på, at der ikke er sket krydsninger mellem neandertalere og den moderne menneskerace.[96]
Mitokondrielt DNA fortæller dog kun om kvindernes udvikling inden for en befolkning og derfor ikke nødvendigvis om hele befolkningens udvikling. Der kan delvist kompenseres for dette ved at undersøge paternelle gensekvenser, f.eks. Y-kromosomets ikke-rekombinerende region.[97] Ikke desto mindre må der inddrages cellekerne-DNA i undersøgelserne for at tegne et mere præcist billede af en befolknings udviklingshistorie.[98]
Funktionsfejl og sygdomme
Mitokondriesygdomme
På grund af mitokondriernes vigtige rolle i cellestofskiftet udgør skader på mitokondrier og deraf følgende funktionsfejl en væsentlig årsag til en række menneskelige sygdomme. Mitokondriesygdomme viser sig ofte som neurologiske forstyrrelser, men kan også føre til myopati, diabetes, multipel endokrinopati samt en række andre systemfejl.[99] Sygdomme forårsaget af mutationer i det mitokondrielle DNA inkluderer Kearns-Sayre-syndrom, MELAS-syndrom og Lebers arvelige opticusneuropati.[100] I hovedparten af tilfældene overføres sygdommen af en kvinde til hendes børn, idet zygoten får sine mitokondrier og dermed sit mtDNA fra ægcellen. Sygdomme som Kearns-Sayre-syndrom, Pearsons syndrom og progressiv ekstern ophthalmoplegi menes at skyldes vidtgående ændringer i mtDNA’et, mens nogle af de andre, såsom MELAS-syndrom, Lebers arvelige opticusneuropati og MERRF (myoclonic epilepsy with ragged red fibers), skyldes punktmutationer i mtDNA.[99]
Ved andre sygdomme fører defekter i cellekernens gener til funktionsfejl hos mitokondriernes proteiner. Dette er tilfældet for Friedreichs ataksi, arvelig spastisk paraplegi samt Wilsons sygdom.[101] Disse sygdomme nedarves dominant ligesom de fleste andre genetiske sygdomme. Mutationer i de af cellekernens gener, der koder for de af mitokondriets enzymer, der foretager oxidativ fosforylering, kan føre til underskud af coenzym Q10 og Barths syndrom.[99] Hvis et individ er prædisponeret for en mitokondriel sygdom, kan miljømæssige faktorer have en udløsende virkning. Eksempelvis menes der at være en forbindelse mellem udsættelse for pesticider og senere udbrud af Parkinsons sygdom.[102][103]
Danske forskere har impliceret mitokondrielt DNA i Parkinsons sygdom.[104] Andre sygdomme med relation til funktionsfejl i mitokondrierne omfatter skizofreni,[105] bipolar affektiv sindslidelse, demens, Alzheimers sygdom,[106] epilepsi, hjerte-kar-sygdom,[107] retinitis pigmentosa og diabetes mellitus.[108][109] Den fælles årsag til disse sygdomme menes at være celleskade som følge af oxidativ stress.
Mitokondrie-medieret oxidativ stress spiller en rolle ved kardiomyopati hos patienter med type-2 diabetes. Øget fedtsyretilførsel til hjertet får fedtsyreoptagelsen i kardiomyocytterne til at stige, hvilket medfører en øget oxidation af fedtsyrer i disse celler. Processen øger mængden af reduktionsækvivalenter (NADH og FADH2) til elektrontransportkæden i mitokondrierne, hvilket kan øge mængden af reaktive iltradikaler, idet flere elektroner ”springer over” elektrontransportkæden og binder sig til ilt. Iltradikalerne øger indstrømningen af hydrogenioner (H+) til matrix via adenin-nukleotid-translokatoren (ANT), således at færre hydrogenioner passerer ATP-syntase-komplekset og bidrager til ATP-syntesen (man siger, at mitokondriet ”frakobles”). Frakoblingen fører til øget iltforbrug i mitokondriet, hvilket øger oxidationen af fedtsyrer. På denne måde starter en selvforstærkende proces, der frakobler mitokondriet yderligere. Selvom iltforbruget stiger, følger ATP-syntesen ikke med, fordi mange af hydrogenionerne som nævnt diffunderer ind i matrix uden at bidrage med energi til ATP-syntesen. Den mindskede ATP-mængde fører til energiunderskud, der svækker muskelsammentrækningen. Problemet forværres af, at det sarkoplasmatiske reticulum får sværere ved at frigive calciumioner (Ca2+), og at mitokondrierne får sværere ved at optage Ca2+, hvilket mindsker mængden af Ca2+ i cytosolen ved sammentrækning. Den mindskede Ca2+-mængde svækker sammentrækningen yderligere; samtidig sænker den aktiviteten af dehydrogenase og dermed også ATP-syntesen.[110]
Mitokondrier og aldringsprocessen
Som nævnt kan de energirige elektroner fra NADH og FADH2 reagere med ilt og danne reaktive iltradikaler, som udsætter mitokondrierne for oxidativ stress. Den oxidative stress mentes at føre til hyppige mutationer i det mitokondrielle DNA (mtDNA).[111] Sammenhængen mellem oxidativ stress og mutationer i mtDNA blev udtænkt allerede i 1956.[112] Den oxidative stress mentes at starte en kædereaktion, idet mutationerne på mtDNA kunne føre til ændret enzymaktivitet og dermed yderligere oxidativ stress. På baggrund af beregninger på antallet af mutationer observeret i mitokondrielt DNA[113] skønnes det dog nu, at der kun sker én mutation i mitokondrielt DNA hvert 7884. år (10-7 til 10-9 pr. base pr. år regnet fra den tidligste stamfar til mennesker og aber), hvilket stemmer overens med skøn over mutationsgraden i autosomalt DNA (10-8 pr. base pr. generation).[114]
Mitokondrier kan undergå forskellige ændringer i forbindelse med aldringsprocessen.[115] Væv fra ældre patienter viser nedsat aktivitet hos enzymerne i respirationskæden.[116] Muteret mtDNA ses dog kun i ca. 0,2 % af meget gamle celler.[117] Sletning af dele af det mitokondrielle genom menes at føre til øget oxidativ stress og hjernecelledød, som kan give Parkinsons sygdom.[118] Debatten går dog på, om mitokondrielle ændringer er årsag til aldringsprocessen eller blot en følge heraf. Et forsøg på mus viste, at flere mutationer i mtDNA førte til forkortet levetid, men ikke en øget mængde iltradikaler.[119] Normale mus ser dog ikke ud til at akkumulere mutationer i deres mtDNA med alderen, hvilket sår tvivl om sammenhængen mellem mutationer i mtDNA og den ”naturlige” aldringsproces.
Se også
Noter
For videnskabelige tidsskrifter angiver volume årgang og issue nummer.
 Denne artikel gengiver public domain-materiale fra NCBI-dokumentet "Science Primer". (engelsk)
Denne artikel gengiver public domain-materiale fra NCBI-dokumentet "Science Primer". (engelsk)
- ^ Taylor, Steven W., et al. 'Characterization of the human heart mitochondrial proteome'. I Nature Biotechnology, volume 21, issue 3 (marts 2003), s. 281–6. DOI:10.1038/nbt793. PMID 12592411. (engelsk)
- ^ Zhang, Jun, et al. 'Systematic Characterization of the Murine Mitochondrial Proteome Using Functionally Validated Cardiac Mitochondria'. I Proteomics, volume 8, issue 8 (2008), s. 1564-1575. DOI:10.1002/pmic.200700851. PMC 2799225. PMID 18348319. (engelsk)
- ^ a b c d e Ernster, Lars, og Gottfried Schatz. 'Mitochondria: a historical review'. I The Journal of Cell Biology, volume 91, issue 3, part 2, 227s–255s. DOI:10.1083/jcb.91.3.227s. PMC 2112799. PMID 7033239. (engelsk)
- ^ Ernster citerer Meves, Friedrich. 'Die Chondriosomen als Träger erblicher Anlagen. Cytologische Studien am Hühnerembryo' (tysk). I Archiv für mikroskopische Anatomie, volume 72, issue 1 (maj 1908), s. 816–867. DOI:10.1007/BF02982402 (Webside ikke længere tilgængelig).
- ^ Siekevitz, Philip. 'Powerhouse of the cell'. I Scientific American, volume 1 (1957), s. 131–140. (engelsk)
- ^ a b c d e f g h i j k Alberts, Bruce, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, og Peter Walter. Molecular Biology of the Cell. New York: Garland Publishing Inc., 1994, ISBN 0-8153-3218-1. (engelsk)
- ^ a b Herrmann, Johannes M., og Walter Neupert. 'Protein transport into mitochondria'. I Current Opinion in Microbiology, volume 3, issue 2 (april 2000), s. 210–214. DOI:10.1016/S1369-5274(00)00077-1. PMID 10744987. (engelsk)
- ^ a b Chipuk, J.E., L. Bouchier-Hayes, og D.R. Green. 'Mitochondrial outer membrane permeabilization during apoptosis: the innocent bystander scenario'. I Cell Death and Differentiation, volume 13, issue 8 (2006), s. 1396–1402. DOI:10.1038/sj.cdd.4401963. PMID 16710362. (engelsk)
- ^ a b c Hayashi, Taruo, et al. 'MAM: more than just a housekeeper'. I Trends in Cell Biology, volume 19, issue 2 (februar 2009), s. 81–8. DOI:10.1016/j.tcb.2008.12.002 Arkiveret 6. marts 2014 hos Wayback Machine. PMC 2750097. PMID 19144519. (engelsk)
- ^ McMillin, Jeanie B., og William Dowhan. 'Cardiolipin and apoptosis'. I Biochimica Et Biophysica Acta, volume 1585, issues 2-3 (december 2002), s. 97–107. DOI:10.1016/S1388-1981(02)00329-3. PMID 12531542. (engelsk)
- ^ Mannella, Carmen A. 'Structure and dynamics of the mitochondrial inner membrane cristae'. I Biochimica Et Biophysica Acta, volume 1763, issues 5-6 (maj-juni 2006), s. 542–548. DOI:10.1016/j.bbamcr.2006.04.006. PMID 16730811. (engelsk)
- ^ Thar, Roland, og Michael Kühl. 'Propagation of electromagetic radiation in mitochondria?' Arkiveret 18. juli 2013 hos Wayback Machine (PDF). I Journal of Theoretical Biology, volume 230, issue 2 (2004), s. 261–270. DOI:10.1016/j.jtbi.2004.05.021. (engelsk)
- ^ a b c d Anderson, S., et al. 'Sequence and organization of the human mitochondrial genome'. I Nature, volume 290, issue 5806 (9. april 1981), s. 427–465. DOI:10.1038/290457a0. PMID 7219534. (engelsk)
- ^ a b c d Rizzuto, Rosario, et al. 'Ca2+ transfer from the ER to mitochondria: when, how and why'. I Biochimica et Biophysica Acta, volume 1787, issue 11 (november 2009), s. 1342–51. DOI:10.1016/j.bbabio.2009.03.015. PMC 2730423. PMID 19341702. (engelsk)
- ^ a b de Brito, Olga Martins, og Luca Scorrano. 'An intimate liaison: spatial organization of the endoplasmic reticulum–mitochondria relationship'. I The EMBO Journal, volume 29, issue 16 (2010), s. 2715–2723. DOI:10.1038/emboj.2010.177. PMC 2924651. PMID 20717141. (engelsk)
- ^ a b Vance, J.E., og Y.J. Shiao. 'Intracellular trafficking of phospholipids: import of phosphatidylserine into mitochondria'. I Anticancer Research, volume 16, issue 3B (1996), s. 1333–9. PMID 8694499. (engelsk)
- ^ a b c Lebiedzinska, Magdalena, et al. 'Interactions between the endoplasmic reticulum, mitochondria, plasma membrane and other subcellular organelles'. I The International Journal of Biochemistry and Cell Biology, volume 41, issue 10 (oktober 2009), s. 1805–16. DOI:10.1016/j.biocel.2009.02.017. PMID 19703651 (engelsk)
- ^ Twig, Gilad, et al. 'Fission and selective fusion govern mitochondrial segregation and elimination by autophagy'. I The EMBO Journal, volume 27, issue 2 (2008), s. 433–446. DOI:10.1038/sj.emboj.7601963. PMC 2234339. PMID 18200046. (engelsk)
- ^ a b c d e Osman, Christof, Dennis R. Voelker, og Thomas Langer. 'Making heads or tails of phospholipids in mitochondria'. I The Journal of Cell Biology, volume 192, issue 1 (2011), s. 7–16. DOI:10.1083/jcb.201006159. PMC 3019561. PMID 21220505. (engelsk)
- ^ Kornmann, Benoît, et al. 'An ER-Mitochondria Tethering Complex Revealed by a Synthetic Biology Screen'. I Science, volume 325, issue 24 (2009), s. 477–481. DOI:10.1126/science.1175088. PMC 2933203. PMID 19556461. (engelsk)
- ^ Rusiñol, A.E., et al. 'A Unique Mitochondria-associated Membrane Fraction from Rat Liver Has a High Capacity for Lipid Synthesis and Contains Pre-Golgi Secretory Proteins Including Nascent Lipoprotein'. I The Journal of Biological Chemistry, volume 269, issue 44 (1994), s. 27494–27502. PMID 7961664. (engelsk)
- ^ (engelsk) Decuypere, Jean-Paul, et al. 'The IP3 receptor–mitochondria connection in apoptosis and autophagy'. I Biochimica et Biophysica Acta, volume 1813, issue 5 (maj 2011), s. 1003–13. DOI:10.1016/j.bbamcr.2010.11.023. PMID 21146562.
- ^ a b Henze, Katrin, og William Martin. 'Evolutionary biology: essence of mitochondria'. I Nature, volume 426, issue 6963 (13. november 2003), s. 127–8. DOI: 10.1038/426127a. PMID 14614484. (engelsk)
- ^ Rappaport, L., P. Oliviero, og J.L. Samuel. 'Cytoskeleton and mitochondrial morphology and function'. I Molecular and Cellular Biochemistry, volume 184, issues 1-2 (1998), s. 101–105. DOI:10.1023/A:1006843113166 (Webside ikke længere tilgængelig). (engelsk)
- ^ Tang, Ho Lam, et al. 'Vimentin supports mitochondrial morphology and organization'. I Biochemical Journal, volume 410, issue 1 (2007), s. 141–6. DOI:10.1042/BJ20071072. PMID 17983357. (engelsk)
- ^ Geneser, Finn, et al. Genesers histologi, 1. udgave, s. 95. København: Munksgaard, 2012, ISBN 978-87-628-0396-1.
- ^ Geneser, Finn, et al. Genesers histologi, 1. udgave, s. 98.
- ^ Campbell, Neil A.; Brad Williamson, og Robin J. Heyden. Biology: Exploring Life. Boston, Massachusetts: Pearson Prentice Hall, 2006. ISBN 0-13-250882-6. (engelsk)
- ^ Alberts, Bruce, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, og Peter Walter. Molecular Biology of the Cell, 5. udgave, s. 824. New York: Garland Publishing Inc., 2008, ISBN 978-0-8153-4106-2. (engelsk)
- ^ a b c d e f Voet, Donald; Judith G. Voet, og Charlotte W. Pratt. Fundamentals of Biochemistry, 2. udgave. John Wiley and Sons, Inc., 2006. (engelsk)
- ^ Rich, P.R. 'The molecular machinery of Keilin's respiratory chain'. I Biochemical Society Transactions, volume 31, part 6 (2003), s. 1095–1105. DOI:10.1042/BST0311095. PMID 14641005. (engelsk)
- ^ Stoimenova, Maria, et al. 'Nitrite-driven anaerobic ATP synthesis in barley and rice root mitochondria'. I Planta, volume 226, issue 2 (2007), s. 465–74. DOI:10.1007/s00425-007-0496-0 (Webside ikke længere tilgængelig). PMID 17333252. (engelsk)
- ^ King, A., M.A. Selak, og E. Gottlieb. 'Succinate dehydrogenase and fumarate hydratase: linking mitochondrial dysfunction and cancer'. I Oncogene, volume 25, issue 34 (2006), s. 4675–4682. DOI:10.1038/sj.onc.1209594. PMID 16892081. (engelsk)
- ^ Huang, Hai, og Kenneth G. Manton. 'The role of oxidative damage in mitochondria during aging: A review'. I Frontiers in Bioscience, volume 9 (2004), s. 1100–1117. DOI:10.2741/1298. PMID 14977532. (engelsk)
- ^ Mitchell, Peter, og Jennifer Moyle. 'Chemiosmotic hypothesis of oxidative phosphorylation'. I Nature, volume 213, issue 5072 (14. januar 1967), s. 137–9. DOI:10.1038/213137a0. PMID 4291593. (engelsk)
- ^ Mitchell, Peter. 'Proton current flow in mitochondrial systems'. I Nature, volume 25, issue 5095 (24. juni 1967), s. 1327-8. DOI:10.1038/2141327a0. PMID 6056845. (engelsk)
- ^ Nobel Foundation. 'Chemistry 1997'. Besøgt 12. september 2012. (engelsk)
- ^ a b Mozo, Julien, et al. 'Thermoregulation: What Role for UCPs in Mammals and Birds?'. I Bioscience Reports, volume 25, issues 3–4 (november 2005), s. 227–249. DOI:10.1007/s10540-005-2887-4 Arkiveret 20. februar 2021 hos Wayback Machine. PMID 16283555.
- ^ Nicholls, David G., og Olov Lindberg. 'Brown-adipose-tissue mitochondria. The influence of albumin and nucleotides on passive ion permeabilities'. I European Journal of Biochemistry, volume 37, issue 3 (1973), s. 523–30. DOI:10.1111/j.1432-1033.1973.tb03014.x. PMID 4777251. (engelsk)
- ^ a b Siegel, George J. (ansvarshavende redaktør), et al. Basic Neurochemistry, 6. udgave. Lippincott Williams & Wilkins, ISBN 0-397-51820-X. (engelsk)
- ^ a b Rossier, Michael F. 'T channels and steroid biosynthesis: in search of a link with mitochondria'. I Cell Calcium, volume 40, issue 2 (2006), s. 155–64. DOI:10.1016/j.ceca.2006.04.020. PMID 16759697. (engelsk)
- ^ Brighton, Carl T., og Robert M. Hunt. 'Mitochondrial calcium and its role in calcification'. I Clinical Orthopaedics and Related Research, volume 100, issue 100 (1973), s. 406–416. DOI:10.1097/00003086-197405000-00057. PMID 4134194. (engelsk)
- ^ Brighton, Carl T., og Robert M. Hunt. 'The role of mitochondria in growth plate calcification as demonstrated in a rachitic model'. I Journal of Bone and Joint Surgery, volume 60-A (1978), s. 630-639. (engelsk)
- ^ Pizzo, Paola, og Tullio Pozzan. 'Mitochondria–endoplasmic reticulum choreography: structure and signaling dynamics'. I Trends in Cell Biology, volume 17, issue 10 (oktober 2007), s. 511–517. DOI:10.1016/j.tcb.2007.07.011 Arkiveret 6. marts 2014 hos Wayback Machine. PMID 17851078. (engelsk)
- ^ Miller, Richard J. 'Mitochondria – the kraken wakes!'. I Trends in Neurosciences, volume 21, issue 3 (marts 1998), s. 95–97. DOI:10.1016/S0166-2236(97)01206-X. (engelsk)
- ^ Green, Douglas R. 'Apoptotic pathways: the roads to ruin'. I Cell, volume 94, issue 6 (september 1998), s. 695–8. DOI:10.1016/S0092-8674(00)81728-6. PMID 9753316. (engelsk)
- ^ (engelsk) Hajnóczky, György, et al. 'Mitochondrial calcium signalling and cell death: approaches for assessing the role of mitochondrial Ca2+ uptake in apoptosis'. I Cell Calcium, volume 40, issues 5–6 (2006), s. 553–60. DOI:10.1016/j.ceca.2006.08.016. PMC 2692319. PMID 17074387.
- ^ a b McBride, Heidi M.; Margaret Neuspiel, og Sylwia Wasiak. 'Mitochondria: more than just a powerhouse'. I Current Biology, volume 16, issue 14 (25. juli 2006), R551–60. DOI:10.1016/j.cub.2006.06.054. PMID 16860735. (engelsk)
- ^ Oh-hama, Tamiko. 'Evolutionary consideration on 5-aminolevulinate synthase in nature'. I Origin of Life and Evolution of Biospheres, volume 27, issue 4 (august 1997), s. 405–12. DOI:10.1023/A:1006583601341 (Webside ikke længere tilgængelig). PMID 9249985. (engelsk)
- ^ Weinberg, Frank, og Chandel, Navdeep S. 'Mitochondrial Metabolism and Cancer'. I Annals of the New York Academy of Sciences, volume 1177, issue 1 (oktober 2009), s. 66–73. DOI:10.1111/j.1749-6632.2009.05039.x. ISSN 0077-8923]. (engelsk)
- ^ Moreno-Sánchez, Rafael, Sara Rodríguez-Enríquez, Alvaro Marín-Hernández, og Emma Saavedra. 'Energy metabolism in tumor cells'. I The FEBS Journal, volume 274, issue 6 (2007), s. 1393–1418. DOI:10.1111/j.1742-4658.2007.05686.x. ISSN 1742-464X. PMID 17302740. (engelsk)
- ^ Pedersen, Peter L. 'ATP Synthase: The machine that makes ATP'. I Current Biology, volume 4, issue 12 (1994), s. 1138–1141. DOI:10.1016/S0960-9822(00)00257-8. ISSN 0960-9822]. (engelsk)
- ^ Pattappa, Girish, Hannah K. Heywood, Joost D. de Bruijn, og David A. Lee. 'The metabolism of human mesenchymal stem cells during proliferation and differentiation'. I Journal of Cellular Physiology, volume 226, issue 10 (2011), s. 2562–2570. DOI:10.1002/jcp.22605. ISSN 0021-9541. (engelsk)
- ^ Agarwal, Bhawana. 'A role for anions in ATP synthesis and its molecular mechanistic interpretation'. I Journal of Bioenergetics and Biomembranes, volume 43, issue 3 (2011), s. 299–310. DOI:10.1007/s10863-011-9358-3 (Webside ikke længere tilgængelig). ISSN 0145-479X]. (engelsk)
- ^ (engelsk) Sweet, S., og G. Singh. 'Changes in mitochondrial mass, membrane potential, and cellular adenosine triphosphate content during the cell cycle of human leukemic (HL-60) cells'. I Journal of Cellular Physiology, volume 180, issue 1 (juli 1999), s. 91–96. DOI:10.1002/(SICI)1097-4652(199907)180:1<91::AID-JCP10>3.0.CO;2-6. ISSN 0021-9541.
- ^ a b Futuyma, D.J. 'On Darwin's Shoulders'. I Natural History, volume 114, issue 9 (2005), s. 64–68. (engelsk)
- ^ Emelyanov, Victor V. 'Mitochondrial connection to the origin of the eukaryotic cell'. I European Journal of Biochemistry, volume 270, issue 8 (2003), s. 1599–1618. DOI:10.1046/j.1432-1033.2003.03499.x. PMID 12694174. (engelsk)
- ^ Gray, Michael W., Gertraud Burger, og B. Franz Lang. 'Mitochondrial evolution'. I Science, volume 283, issue 5407 (marts 1999), 1476–81. DOI:10.1126/science.283.5407.1476. PMID 10066161. (engelsk)
- ^ Thrash, J. Cameron, et al. 'Phylogenomic evidence for a common ancestor of mitochondria and the SAR11 clade'. I Scientific Reports, volume 1 (juni 2011). DOI:10.1038/srep00013. (engelsk)
- ^ O'Brien, Thomas W. 'Properties of human mitochondrial ribosomes'. I IUBMB Life, volume 55, issue 9 (september 2003), s. 505–13. DOI:10.1080/15216540310001626610. PMID 14658756. (engelsk)
- ^ Sagan, Lynn. 'On the origin of mitosing cells'. I Journal of Theoretical Biology, volume 14, issue 3 (marts 1967), s. 255–274. DOI:10.1016/0022-5193(67)90079-3. PMID 11541392. (engelsk)
- ^ Emelyanov, Victor V. 'Rickettsiaceae, rickettsia-like endosymbionts, and the origin of mitochondria'. I Bioscience Reports, volume 21, issue 1 (2001), s. 1–17. DOI:10.1023/A:1010409415723 Arkiveret 20. februar 2021 hos Wayback Machine. PMID 11508688. (engelsk)
- ^ Feng, Da-Fei, Glen Cho, og Russell F. Doolittle. 'Determining divergence times with a protein clock: Update and reevaluation'. I Proceedings of the National Academy of Sciences of the United States of America, volume 94, issue 24 (november 1997), s. 13028–13033. DOI:10.1073/pnas.94.24.13028. PMC 24257. PMID 9371794. (engelsk)
- ^ Cavalier-Smith, T. 'Archamoebae: the ancestral eukaryotes?'. I Biosystems, volume 25, issues 1–2 (1991), s. 25–38. DOI:10.1016/0303-2647(91)90010-I. PMID 1854912. (engelsk)
- ^ Andersson, G.E.; Olof Karlberg, Björn Canbäck, og Charles G. Kurland. 'On the origin of mitochondria: a genomics perspective'. I Philosophical Transactions of The Royal Society of London, B, Biological Sciences, volume 358, issue 1429 (januar 2003), s. 165–77; diskussion s. 177–9. DOI:10.1098/rstb.2002.1193. PMC 1693097. PMID 12594925. (engelsk)
- ^ a b c d Chan, David C. 'Mitochondria: Dynamic Organelles in Disease, Aging, and Development'. I Cell, volume 125, issue 7 (30. juni 2006), s. 1241-1252. DOI:10.1016/j.cell.2006.06.010. PMID 16814712. (engelsk)
- ^ Wiesner, Rudolf J., Caspar J. Rüegg, og Ingo Morano. 'Counting target molecules by exponential polymerase chain reaction, copy number of mitochondrial DNA in rat tissues'. I Biochimica Et Biophysica Acta, volume 183, issue 2 (1992), s. 553–559. DOI:10.1016/0006-291X(92)90517-O. PMID 1550563. (engelsk)
- ^ a b Geneser, Finn, et al. Genesers histologi, 1. udgave, s. 97.
- ^ Fukuhara, H. et al. 'Linear mitochondrial DNAs of yeasts: frequency of occurrence and general features'. I Molecular and Cellular Biolology, volume 13, issue 4 (april 1993), s. 2309–2314. PMC 359551. PMID 8455612. (engelsk)
- ^ Bernardi, Giorgio. 'Intervening sequences in the mitochondrial genome'. I Nature, volume 276, issue 5688 (7. december 1978), s. 558–559. DOI:10.1038/276558a0. PMID 214710. (engelsk)
- ^ Hebbar, Sharda K., Scott M. Belcher, og Philip S. Perlman. 'A maturase-encoding group IIA intron of yeast mitochondria self-splices in vitro'. I Nucleic Acids Research, volume 20, issue 7 (april 1992), s. 1747–54. DOI:10.1093/nar/20.7.1747. PMC 312266. PMID 1579468. (engelsk)
- ^ Gray, Michael W., et al. 'Genome structure and gene content in protist mitochondrial DNAs'. I Nucleic Acids Research, volume 26, issue 4 (februar 1998), s. 865–878. DOI:10.1093/nar/26.4.865. PMC 147373. PMID 9461442. (engelsk)
- ^ Gray, Michael W., B. Franz Lang, og Gertraud Burger. 'Mitochondria of protists'. I Annual Reviews of Genetics, volume 38 (2004), s. 477–524. DOI:10.1146/annurev.genet.37.110801.142526 Arkiveret 2. juni 2016 hos Wayback Machine. PMID 15568984. (engelsk)
- ^ Shao, Renfu, Ewen F. Kirkness, og Stephen C. Barker. 'The single mitochondrial chromosome typical of animals has evolved into 18 minichromosomes in the human body louse, Pediculus humanus'. I Genome Research, volume 19, issue 5 (marts 2009), s. 904–12. DOI:[http://genome.cshlp.org/content/19/5/904 10.1101/gr.083188.108. PMC 2675979. PMID 19336451. (engelsk)
- ^ Crick, Francis H.C., og L.E. Orgel. 'Directed panspermia'. I Icarus, volume 19 (1973), s. 341-346. Citat s. 344: "It is a little surprising that organisms with somewhat different codes do not coexist." (Se 29+ Evidences for Macroevolution: Part 1 for yderligere information). (engelsk)
- ^ Barrell, B.G., A.T. Bankier, og J. Drouin. 'A different genetic code in human mitochondria'. I Nature, volume 282, issue 5735 (1979), s. 189–194. DOI:10.1038/282189a0. PMID 226894. (engelsk)
- ^ Se 'The Genetic Codes'. Compiled by Andrzej (Anjay) Elzanowski and Jim Ostell. National Center for Biotechnology Information (NCBI), Bethesda, Maryland, USA (engelsk).
- ^ Jukes, T.H., og S. Osawa. 'The genetic code in mitochondria and chloroplasts'. I Experientia, volume 46, issues 11–12 (1. december 1990), s. 1117–26. DOI:10.1007/BF01936921 (Webside ikke længere tilgængelig). PMID 2253709. (engelsk)
- ^ Hiesel, R., B. Wissinger, W. Schuster, A. Brennicke. 'RNA editing in plant mitochondria'. I Science, volume 246, issue 4937 (2006), s. 1632–4. 10.1126/science.2480644. PMID 2480644. (engelsk)
- ^ Abascal, Federico, David Posada, Robin D. Knight, og Rafael Zardoya. 'Parallel Evolution of the Genetic Code in Arthropod Mitochondrial Genomes'. I PLoS Biology, volume 4, issue 5 (2006), s. 0711–0718. DOI:10.1371/journal.pbio.0040127 Arkiveret 6. marts 2014 hos Wayback Machine. PMC 1440934. PMID 16620150. (engelsk)
- ^ Henriquez, Fiona L., et al. 'The unusual mitochondrial compartment of Cryptosporidium parvum'. I Trends in Parasitology, volume 21, issue 2 (februar 2005), s. 68–74. DOI:10.1016/j.pt.2004.11.010 Arkiveret 6. marts 2014 hos Wayback Machine. PMID 15664529. (engelsk)
- ^ Hermann, Greg J., et al. 'Mitochondrial Fusion in Yeast Requires the Transmembrane GTPase Fzo1p'. I The Journal of Cell Biology, volume 143, issue 2 (oktober 1998), s. 359–373. DOI:10.1083/jcb.143.2.359. PMC 2132826. PMID 9786948. (engelsk)
- ^ Seo, Arnold Y., et al. 'New insights into the role of mitochondria in aging: mitochondrial dynamics and more'. I Journal of Cell Science, volume 123, issue 15 (august 2010), s. 2533–42. DOI:10.1242/jcs.070490. PMC 2912461. PMID 20940129. (engelsk)
- ^ Kimball, J.W. 'Sexual Reproduction in Humans: Copulation and Fertilization', Kimball's Biology Pages (2006) (baseret på Biology, 6th edition, 1996). (engelsk)
- ^ Sutovsky, Peter, et al. (1999). 'Ubiquitin tag for sperm mitochondria'. I Nature, volume 402, issue 6760 (november 1999), s. 371–372. DOI:10.1038/46466. PMID 10586873. (engelsk)
- ^ Mogensen, H. Lloyd. 'The Hows and Whys of Cytoplasmic Inheritance in Seed Plants'. I American Journal of Botany, volume 83, issue 3 (marts 1996), s. 383–404. 10.2307/2446172. JSTOR 2446172. (engelsk)
- ^ Johns, Donald R. 'Paternal transmission of mitochondrial DNA is (fortunately) rare'. I Annals of Neurology, volume 54, issue 4 (2003), s. 422–4. DOI:10.1002/ana.10771. PMID 14520651. (engelsk)
- ^ Se 'Fruit flies offer DNA clue to why women live longer'. (engelsk) BBC Health, 2. august 2012.
- ^ Thyagarajan, Bhaskar, Rodolfo A. Padua, og Colin Campbell. 'Mammalian mitochondria possess homologous DNA recombination activity'. I The Journal of Biological Chemistry, volume 271, issue 44 (1996), s. 27536–27543. DOI:10.1074/jbc.271.44.27536. PMID 8910339. (engelsk)
- ^ Lunt, David H., og Bradley C. Hyman. 'Animal mitochondrial DNA recombination'. I Nature, volume 387, issue 6630 (15. maj 1997), s. 247. DOI:10.1038/387247a0. PMID 9153388. (engelsk)
- ^ Eyre-Walker, Adam, Noel H. Smith, og John Maynard Smith. 'How clonal are human mitochondria?'. I Proceedings of The Royal Society of London, B, Biological Sciences, volume 266, issue 1418 (marts 1999), s. 477–483. DOI:10.1098/rspb.1999.0662. PMC 1689787. PMID 10189711. (engelsk)
- ^ Awadalla, Philip, Adam Eyre-Walker, og John Maynard Smith. 'Linkage Disequilibrium and Recombination in Hominid Mitochondrial DNA'. I Science, volume 286, issue 5449 (24. december 1999), s. 2524–2525. DOI:10.1126/science.286.5449.2524. PMID 10617471. (engelsk)
- ^ Castro, J.A., A. Picornell, og M. Ramon. 'Mitochondrial DNA: a tool for populational genetics studies'. I International Microbiology, volume 1, issue 4 (1998), s. 327–32. PMID 10943382. (engelsk)
- ^ Cann, Rebecca L., Mark Stoneking, og Allan C. Wilson. 'Mitochondrial DNA and human evolution'. I Nature, volume 325, issue 6099 (januar 1987), s. 31–36. DOI:10.1038/325031a0. PMID 3025745. (engelsk)
- ^ Torroni, Antonio, et al. 'Harvesting the fruit of the human mtDNA tree'. I Trends in Genetics, volume 22, issue 6 (juni 2006), s. 339–45. DOI:10.1016/j.tig.2006.04.001. PMID 16678300. (engelsk)
- ^ Krings, Matthias, et al. 'Neandertal DNA sequences and the origin of modern humans'. I Cell, volume 90, issue 1 (juli 1997), s. 19–30. DOI:10.1016/S0092-8674(00)80310-4. PMID 9230299. (engelsk)
- ^ Garrigan, D., og M.F. Hammer. 'Reconstructing human origins in the genomic era'. I Nature Reviews: Genetics, volume 7, issue 9 (2006), s. 669–80. DOI:10.1038/nrg1941. PMID 16921345. (engelsk)
- ^ Harding, R.M., et al. 'Archaic African and Asian lineages in the genetic ancestry of modern humans'. I American Journal of Human Genetics, volume 60, issue 4 (april 1997), s. 772–89. PMC 1712470. PMID 9106523. (engelsk)
- ^ a b c Zeviani, Massiano, og Stefano Di Donato. 'Mitochondrial disorders'. I Brain, volume 127, part 1 (2004), s. 2153–2172. DOI:10.1093/brain/awh259. PMID 15358637. (engelsk)
- ^ Taylor, William R., og Doug M. Turnbull. 'MITOCHONDRIAL DNA MUTATIONS IN HUMAN DISEASE'. I Nature Reviews Genetics, volume 6, issue 5 (2005), s. 389–402. DOI:10.1038/nrg1606. PMC 1762815. PMID 15861210. (engelsk)
- ^ Chinnery, P.F., og E.A. Schon. 'Mitochondria'. I Journal of Neurology, Neurosurgery and Psychiatry, volume 74, issue 9 (2003), s. 1188–99. DOI:10.1136/jnnp.74.9.1188. PMC 1738655. PMID 12933917. (engelsk)
- ^ Sherer, Todd B., Ranjita Betarbet, og J. Timothy Greenamyre. 'Environment, mitochondria, and Parkinson's disease'. I The Neuroscientist, volume 8, issue 3 (2002), s. 192–7. DOI:10.1177/1073858402008003004. PMID 12061498. (engelsk)
- ^ Gomez C., M.J. Bandez, og A. Navarro. 'Pesticides and impairment of mitochondrial function in relation with the parkinsonian syndrome'. I Frontiers in Bioscience, volume 12 (2007), s. 1079–93. DOI:10.2741/2128. PMID 17127363. (engelsk)
- ^ Mitochondrial DNA damage triggers spread of Parkinson’s disease-like pathology. Nature 2023
- ^ Gardner, Ann, og Richard G. Boles. 'Is a "Mitochondrial Psychiatry" in the Future? A Review'. I Current Psychiatry Review, volume 1, issue 3 (2005), s. 255–271. DOI:10.2174/157340005774575064. (engelsk)
- ^ Lim, Yun-An, et al. 'Abeta and human amylin share a common toxicity pathway via mitochondrial dysfunction'. I Proteomics, volume 10, issue 8 (2010), s. 1621–33. DOI:10.1002/pmic.200900651. PMID 20186753. (engelsk)
- ^ Lesnefsky, Edward J., et al. 'Mitochondrial dysfuntion in cardiac disease: ischemia-reperfusion, aging and heart failure'. I Journal of Molecular and Cellular Cardiology, volume 33, issue 6 (juni 2001), s. 1065–1089. DOI:10.1006/jmcc.2001.1378. PMID 11444914. (engelsk)
- ^ Schapira, Anthony H.V. 'Mitochondrial disease'. I The Lancet, volume 368, issue 9529 (2006), s. 70–82. DOI:10.1016/S0140-6736(06)68970-8. PMID 16815381. (engelsk)
- ^ Pieczenik, Steve R., og John Neustadt. 'Mitochondrial dysfunction and molecular pathways of disease'. I Experimental and Molecular Pathology, volume 83, issue 1 (august 2007), s. 84–92. DOI:10.1016/j.yexmp.2006.09.008. PMID 17239370. (engelsk)
- ^ Bugger, Heiko, og E. Dale Abel. 'Mitochondria in the diabetic heart'. I Cardiovascular Research, volume 88, issue 2 (2010), s. 229–240. DOI:10.1093/cvr/cvq239. (engelsk)
- ^ Richter, C., J. Park, og B.N. Ames. 'Normal oxidative damage to mitochondrial and nuclear DNA is extensive'. I Proceedings of the National Academy of Sciences of the United States of America, volume 85, issue 17 (september 1988), s. 6465–6467. DOI:10.1073/pnas.85.17.6465. PMC 281993. PMID 3413108. (engelsk)
- ^ Harman, D. 'Aging: a theory based on free radical and radiation chemistry'. I Journal of Gerontology, volume 11, issue 3 (1956), s. 298–300. PMID 13332224. (engelsk)
- ^ Soares, Pedro, et al. 'Correcting for Purifying Selection: An Improved Human Mitochondrial Molecular Clock'. I American Journal of Human Genetics, volume 84, issue 6 (12. juni 2009), s. 740–759. (engelsk)
- ^ Nachman, Michael W., og Susan L. Crowell. 'Estimate of the Mutation Rate per Nucleotide in Humans'. I Genetics, volume 156 (september 2000), s. 297-304. (engelsk)
- ^ Se 'Mitochondria and Aging' (engelsk).
- ^ Boffoli, D., et al. 'Decline with age of the respiratory chain activity in human skeletal muscle'. I Biochimica et Biophysica Acta, volume 1226, issue 1 (1994), s. 73–82. DOI:10.1016/0925-4439(94)90061-2. PMID 8155742. (engelsk)
- ^ de Grey, Aubrey. 'Mitochondrial Mutations in Mammalian Aging: An Over-Hasty About-Turn?' I Rejuvenation Research, volume 7, issue 3 (efterår 2004), s. 171–4. DOI:10.1089/rej.2004.7.171. PMID 15588517. (engelsk)
- ^ Bender, A., et al. 'High levels of mitochondrial DNA deletions in substantia nigra neurons in aging and Parkinson disease'. I Nature Genetics, volume 38, issue 5 (2006), s. 515–517. DOI:10.1038/ng1769. PMID 16604074. (engelsk)
- ^ Trifunovic, Aleksandra, et al. 'Somatic mtDNA mutations cause aging phenotypes without affecting reactive oxygen species production'. I Proceedings of the National Academy of Sciences of the United States of America, volume 102, issue 50 (2005), s. 17993–8. DOI:10.1073/pnas.0508886102. PMC 1312403. PMID 16332961. (engelsk)
Eksterne henvisninger
- Mitokondrie-atlas Arkiveret 29. juni 2012 hos Wayback Machine fra Mainz' Universitet (engelsk)
- Mitokondrieforskningsportal på mitochondrial.net (engelsk)
- Mitochondria: Architecture dictates function Arkiveret 25. januar 2010 hos Wayback Machine på cytochemistry.net (engelsk)
- Mitokondrielinks Arkiveret 18. april 2009 hos Wayback Machine fra University of Alabama (engelsk)
- MIP Mitochondrial Physiology Society (engelsk)
- 3D-strukturer af proteiner fra mitokondriets indermembran fra University of Michigan (engelsk)
- 3D-strukturer af proteiner i mitokondriets ydermembran fra University of Michigan (engelsk)
- Mitochondrial Protein Partnership fra University of Wisconsin (engelsk)
- Mitochondrion – Cell Centered Database (engelsk)
- Mitokondrie rekonstrueret ved elektrontomografi fra San Diego State University (engelsk)
- Videoklip af mitokondrie fra rottelever med kryo-elektron-tomografi Arkiveret 11. december 2003 hos Wayback Machine (engelsk)
Medier brugt på denne side
Forfatter/Opretter: MesserWoland og Szczepan1990, Licens: CC BY-SA 3.0
Skematisk tegning af en typisk dyrecelle og dens organeller:
- Nukleolus
- Nukleus
- Ribosomer (små prikker)
- Vesikel
- Endoplasmatisk reticulum
- Golgiapparattet
- Cytoskelet
- Granulært (ru) Glat endoplasmatisk reticulum
- Mitokondrier
- Vakuol
- Cytosol
- Lysosom
- Centrioler
Transmission electron microscope image of a thin section cut through an area of mammalian lung tissue. The high magnification image shows two mitochondria.
JEOL 100CX TEMThis is an image of a frozen-hydrated rat liver mitochondrion based on work done at the Wadsworth Center's Resource for Visualization of Biological Complexity (http://www.wadsworth.org/databank/electron/cryomito_dis2.html). It has not been previously published and I am releasing it into public domain for this article. The point is that the cristae are not folds of the inner membrane of the mitochondrion but pleomorphic invaginations with narrow tubular connections to each other and to the peripheral region of the inner membrane. I can advise on how to change your cartoon to be more accurate, while still retaining the basic format. There are numerous published references in last 10 years, the most recent: C.A. Mannella (2006) Biophysica et Biochimica Acta 1762: 140-147
Skematisk tegning af elektrontransportkæden i mitokondriets indermembran
Forfatter/Opretter:
- derivative work: Shanel (diskussion)
Structure of the human mitochondrial genome.
Forfatter/Opretter: Robert M. Hunt, Licens: CC BY-SA 3.0
Transmission electron micrograph of a chondrocyte, stained for calcium, showing its nucleus (N) and mitochondria (M).
A diagram showing a mitochondrion of the eukaryotic cell. Mitochondria are organelles surrounded by membranes, distributed in the cytosol of most eukaryotic cells. Its main function is the conversion of potential energy of pyruvate molecules into ATP.