Lipopolysaccharid
Lipopolysaccharider, LPS, lipoglycaner eller endotoksiner er glycolipider, der udgør hovedbestanddelen af den ydre membran af gram-negative bakterier. LPS er store molekyler bestående af Lipid A, et lipid forankret i den ydre membran og et polysaccharid sammensat af tre dele: O-antigen, ydre kerne og indre kerne, jf. billederne.[1]
LPS er meget aktive biologiske molekyler og kaldes også endotoxin på grund af Lipid A-delens stærke toksiske virkning. LPS er et exogent pyrogen (feberfremkalder). LPS inducerer desuden et stærkt respons fra immunsystemet. Det kræver ikke nødvendigvis ødelæggelsen af den bakterielle cellevæg, idet LPS udskilles fra bakterien som en del af den normale fysiologiske aktivitet som såkaldte ydre membran-vesikler (en. OMV).[2][3]
Generelt

LPS er hovedkomponenten i den ydre membran af gram-negative bakterier (se billedet), hvilket bidrager betragteligt til bakteriens strukturelle integritet og beskytter membranen mod visse typer kemiske angreb. LPS øger også den negative ladning af cellemembranen og hjælper med at stabilisere den samlede membranstruktur.[4] LPS tilstedeværelse og integritet på den ydre membran er af afgørende betydning for mange gram-negative bakterier, som dør, hvis LPS er muteret eller fjernet.[5]
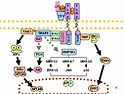
De gram-negative bakterier danner deres LPS på den indre membran, transporterer det igennem periplasmaet og translokerer det igennem den ydre membran (se billederne).[4]
O-serotyper
O-kæden er eksponeret på den yderste overflade af bakteriecellen og er som en følge heraf et mål for immunsystemet.[4] Den kemiske opbygning af O-kæden varierer fra bakterie til bakterie og giver sero-specificiteten. O-kæden er opbygget af 50-100 enheder bestående af en eller flere monosaccharider, og der er stor variation mellem bakteriestammerne i kombinationen, positionen, stereokemien, bindingerne og tilstedeværelsen eller fraværet af andre enheder end saccharider. For eksempel er der over 196 forskellige O-antigenstrukturer produceret af forskellige E. coli-stammer. Bakterier uden eller med kortkædet LPS har sædvanligvis en ydre membran, der er mere gennemtrængelig for hydrofobe antibiotika.[4][5][6]
O-serotyperne af bakterier blev etableret af Fritz Kauffmann og udarbejdet af Ida Ørskov og Frits Ørskov på Statens Seruminstitut.[7]
Kernen
Kernen kaldes også “core-domænet” og er altid en oligosaccharidkomponent af 9-12 saccharider, der er knyttet direkte til Lipid A. Den kan almindeligvis deles op i den ydre og indre kerne på basis af hhv. sukkerarterne heptose og KDO, 3-deoxy-D-manno-oct-2-ulosonsyre (også kendt som keto-deoxyoctulosonat). LPS-kernen af mange bakterier indeholder også ikke-kulhydratbestanddele, såsom phosphat, aminosyrer og ethanolamin-forbindelser.[4][6]
Lipid A
Lipid A er den komponent af et endotoxin, der er ansvarlig for gram-negative bakteriers toksicitet. Detekteringen af både lipid A og O-antigen af det humane immunsystem kan være kritisk for starten af immunresponset på en gram-negativ infektion og for den efterfølgende vellykkede bekæmpelse af infektionen.[4][6]
Lipid A består af to glucosamin-enheder, i en β (1 → 6) binding, med seks tilknyttede acylkæder, fedtsyrer, og indeholder desuden en phosphatgruppe på hvert kulhydrat. Det er acylkæderne der er forankret i membranen. Lipid A fra E. coli har som et eksempel typisk fire C14 hydroxyacyl-kæder bundet direkte til glucosaminerne og en C14 og en C12 bundet til beta-hydroxygrupperne jf. billedet.[4][6]
Immunresponset
Mange af LPS’ immunaktiverende egenskaber kan tilskrives lipid A-enheden. Det er meget stærkt stimulerende for immunsystemet ved at aktivere immunceller selv ved ganske små koncentrationer omkring picogram pr. milliliter. De berørte immunceller er især monocytter, dendritceller, makrofager og B-celler, og responset består i sekretion af pro-inflammatoriske cytokiner, nitrogenmonooxid og eicosanoider. Immuncellerne har to specielle receptorer, der erkender LPS, CD14 og Toll-lignende receptorer, TLR (bemærk den specielle historie bag navnet).[8]
Primært er receptorerne TLR4 og CD14 plus MD-2 på celleoverfladen påkrævet for aktivering af det medfødte immunsystem ved erkendelse af LPS fra gramnegative bakterier. TLR4/MD-2 systemets evne til at reagere specielt på Lipid A er klinisk vigtig.[4][5][6]
| Lipopolysaccharid | |||||||||
| |||||||||
Henvisninger
- ^ Bacterial endotoxin-lipopolysaccharide; structure, function and its role in immunity in vertebrates and invertebrates. Agriculture and Natural Resources 2018
- ^ "Så meget endotoksin udsættes vi for. Det nationale forskningscenter for arbejdsmiljø 2006". Arkiveret fra originalen 21. oktober 2020. Hentet 20. oktober 2020.
- ^ Hypotese: Sådan kan dine tarmbakterier gøre dig ekstra tyk. Videnskab.dk 2016
- ^ a b c d e f g h "Lipopolysaccharide Endotoxins. Annual Reviews 2002". Arkiveret fra originalen 7. juli 2019. Hentet 7. juli 2019.
- ^ a b c Pushing the envelope: LPS modifications and their consequences. Nature Reviews Microbiology 2019
- ^ a b c d e Lipopolysaccharide modification in Gram-negative bacteria during chronic infection. FEMS Microbiology Reviews 2016
- ^ Serology, chemistry, and genetics of O and K antigens of Escherichia coli. Bacteriol. Rev. 1977
- ^ The Nobel Prize in Physiology or Medicine 1995
Medier brugt på denne side
Forfatter/Opretter: en:User:Lmaps and User:TimVickers, Licens: CC BY-SA 3.0
Structure of the (3-deoxy-D-manno-octulosonic acid)2 Lipid A endotoxin from E. coli K-12
Forfatter/Opretter: Jeff Dahl, Licens: CC BY-SA 4.0
Diagram of a gram-negative cell wall.
Forfatter/Opretter: Mike Jones, Licens: CC BY-SA 3.0
LPS Transport
Completed LPS molecules are transported to the outer leaflet of the outer membrane from the periplasmic side of the inner membrane by a consortium of Lpt proteins. The inner membrane LptB2CFG complex uses cytoplasmic ATP, to energise entire mechanism of transport. LptA is a periplasmic protein that shuttles the LPS to the outer membrane. The LptDE complex places the LPS in the outer leaflet. The precise biochemical functions of these proteins is not known, function is infered by deletion mutations.
Review of the subject N. Ruiz et al. (2009) Nature Reviews Microbiology 7(9), pp.677-83Forfatter/Opretter: Mike Jones, Licens: CC BY-SA 3.0
Structure and synthesizing enzymes of Escherichia coli R1 core oligosaccharide: Green indicates residues that constitute the inner core. Blue indicates residues that constitute the outer core.
Simple representation of the toll-like receptor pathways, taken from my seminar powerpoint. Revised to include TIRAP/Mal. Dashed grey lines represent unknown associations. Les cadenes LPS representen lipopolisacàrids.
Forfatter/Opretter: Mike Jones, Licens: CC BY-SA 3.0
LPS final assembly. On the left of the diagram, O-antigen assembly. O-antigen subunits are assembled on the cytoplasmic side of the inner membrane, translocated across the inner membrane by the Wzx flipase and polymerized by the Wzy polymerase (chain length controlled by Wzz). Completed Core-Lipid A units are translocated to the periplasm by the MsbA flipase. O-antigen and Lipid A are ligated by WaaL ligase, producing a complete LPS on the periplasmic side of the inner membrane.