Kritisk micellekoncentration
| Hvad handler artiklen om? Denne artikels indledning bør kort forklare, hvad artiklen handler om, jf. stilmanualen. Husk at skrive det indlysende. |
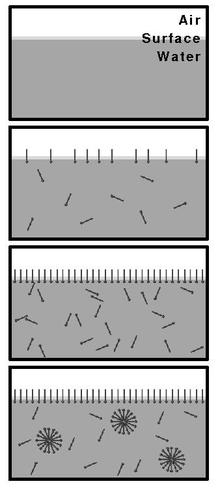
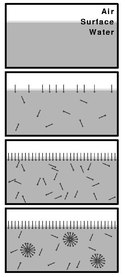
Den kritiske aggregeringskoncentration (CAC) eller traditionelt den kritiske micellekoncentration (CMC) er den koncentration, hvor surfaktanter i en opløsning begynder at danne aggregater i form af fx miceller. Surfaktanter er molekyler, der kan sætte sig på opløsningens overflade og derved nedsætte overfladespændingen. Aggregater er i denne sammenhæng strukturer, der består af flere surfaktanter.[1][2]
I begyndelsen vil en opløsnings overfladespænding falde i takt med, at koncentrationen af surfaktanter øges. Når koncentrationen er lig med CMC, vil overfladespændingen derimod opnå en konstant værdi eller i hvert fald fald ændres betydeligt langsommere, da tilførte surfaktanter i stedet danner miceller. Eksperimentelt kan CMC altså bestemmes ved at måle overfladespændingen som funktion af koncentrationen. CMC afhænger af temperatur, tryk og tilstedeværelsen af andre overfladeaktive elementer samt elektrolytter. Miceller dannes kun over den kritiske micelletemperatur.
Fx er CMC for surfaktanten SDS i rent vand ved 25 °C og atmosfærisk tryk målt til mol/L.[3]
Kildehenvisninger
- ^ (engelsk) International Union of Pure and Applied Chemistry. "critical micelle concentration". Compendium of Chemical Terminology Internet-udgave.
- ^ Israelachvili, Jacob N. (2011). "19.5 The Critical Micelle Concentration (CMC)". Intermolecular and Surface Forces (engelsk) (3. udgave). Academic Press. p. 512-513. ISBN 978-0-12-375182-9.
- ^ Ana Domínguez, Aurora Fernández, Noemí González, Emilia Iglesias, and Luis Montenegro "Determination of Critical Micelle Concentration of Some Surfactants by Three Techniques", Journal of Chemical Education, Vol. 74 No. 10 October 1997, pp. 1227–1231 (pdf)
| Spire Denne artikel om fysik er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
Medier brugt på denne side
Forfatter/Opretter: Schmin, Licens: CC BY-SA 3.0
Increasing concentration of surfactant in water eventually forms micelles at or above critical micelle concentration.
Nuclear physics