Henfaldskæde
I kernefysik, betegner henfaldskæder en sammenhængende kæde af radioaktive henfald. De fleste radioisotoper henfalder ikke direkte til en stabil tilstand, men gennemløber en serie af henfald, indtil en stabil isotop er dannet. Et led i en henfaldskæde betegnes ved dens relation til foregående eller efterfølgende trin. En “forældre-isotop" gennemgår henfald til en “datter-isotop”. Et eksempel er uran (atom nummer 92), som henfalder til thorium (atom nummer 90). Datter-isotopen kan være stabil eller kan henfalde og danne sin egen datter-isotop. Datteren af en datter kaldes nogle gange ”datter-datter isotop”.
Tiden, som det tager for et forældre-atom at henfalde til et atom af dets datter-isotop varierer meget, ikke kun for forskellige forældre-datter kæder, men også for ens par af forældre og datter-isotoper. Mens henfaldet af et enkelt atom sker spontant, er henfaldet af en start-population af identiske atomer i tiden ”t”, beskrevet ved en aftagende eksponentiel fordeling, e−λt, hvor λ kaldes henfaldskonstanten. På grund af den eksponentielle sammenhæng, kan man beskrive isotopen ved halveringstiden.
Halveringstiden er den tid det tager for halvdelen af et oprindeligt antal af forældre-isotoper at henfalde til deres datter-isotop. Halveringstider er blevet bestemt eksperimentelt for tusinder af radio-isotoper. De varierer fra næsten øjeblikkeligt henfald til 1019 år, eller længere.
De mellemliggende trin udsender den samme mængde af radioaktivitet som den oprindelige isotop (dog ikke den samme energi). Når der opnås ligevægt, vil en datter-isotop være tilstede i direkte forhold til dens halveringstid; men da dens aktivitet er omvendt proportional med halveringstiden, vil hvert nuklid i henfaldskæden til sidst bidrage med lige så meget radioaktivitet som isotopen i begyndelsen af kæden, men ikke med den samme energi. For eksempel er uran-238 svagt radioaktivt, mens begblende, en uranmalm, er 13 gange mere radioaktivt end rent uran i samme mængde, på grund af radium og andre datter-isotoper som det indeholder.
Ustabile radium isotoper er ikke kun vigtige radioaktive kilder, men som det næste led i kæden frembringer de radon,en inaktiv, naturligt forekommende gas. Klipper som indeholder thorium og/eller uran (som nogle granitter) udsender radon gas, der kan opsamles i lukkede steder som kældre og miner under jorden. Udsættelse for radon anses for at være den vigtigste årsag til lungekræft i ikke-rygere. .[1]
Historie
Alle de grundstoffer og isotoper som vi finder på Jorden, med undtagelse af hydrogen, deuterium, helium, helium-3, og måske små mængder af stabile lithium og beryllium isotoper, som blev skabt i Big Bang, blev dannet ved s-proces eller r-proces i stjerner. Dem som i dag findes på Jorden, kan derfor senest være dannet for 4.5 milliarder år siden. Alle grundstoffer som er skabt for mere end 4.5 milliarder år siden kaldes “primordiale”, hvilket betyder at de er dannet ved processer i stjerner. Ved dannelses-tidspunktet, begyndte de ustabile grundstoffer at henfalde med det samme. Alle isotoper med halveringstid mindre end 100 millioner år er reduceret til 0.0000000000028% (2.8×10−12%) eller mindre af de oprindelige mængder, som var i Jorden ved dens dannelse. De findes i spormængder i dag, eller er henfaldet helt. Der er kun to andre måder at lave isotoper: ”kunstigt”, inden i en menneskeskabt eller naturlig reaktor, eller gennem henfald af en forældre-isotop i en henfaldskæde.
Ustabile isotoper forsøger at blive stabile; deres mål er at blive en af de 200 stabile isotoper der findes i universet. Stabile isotoper har et forhold mellem neutroner og protoner i kernen der er 1 i stabilt helium-4 og langsomt vokser til ca. 1.5 for bly. (der er ingen fuld stabilitet for isotoper tungere end bly-208). Grundstoffer som er tungere end det, skal af med noget masse for at opnå stabilitet, oftest som alfahenfald. Den anden almindelige måde for et isotop med den rette masse, men med et højt neutron-proton forhold (n/p) er betahenfald, i hvilket der sker grundstof-forvandling, mens massen er bevaret og n/p bliver mindre.
Der findes også et inverst beta henfald, der hjælper isotoper med for få neutroner til at nærme sig stabilitet; men da fission næsten kun har produkter som er neutron-tunge er positron emission relativt sjælden sammenlignet med beta emission.
Der er mange relativt korte betahenfaldskæder, mindst to (et tungt betahenfald og et let positron henfald) for hver masse op til omkring 207 og nogle højere, men for de tungere grundstoffer (ofte kaldet "transuraner", men faktisk brugt for alle isotoper tungere end bly) er der kun 4 meget sandsynlige henfaldskæder.
Denne kendsgerning skyldes de to mulige henfald: Alfahenfald, der reducerer massen med 4 AMU, og beta, der ikke ændrer massen, men kun p/n forholdet. De fire kæder kaldes 4n + 1, 4n + 2, and 4n + 3; resten, som fås ved at dividere atommassen med 4 giver den kæde som isotopen vil bruge til henfald.
Der er andre muligheder, men de har en meget lavere sandsynlighed for at forekomme end alfa- eller betahenfald.
Tre af disse kæder har en lang-livet isotop nær starten af kæden; de er flaskehalse i processen, der sænker hastigheden i henfaldskæden og holder kæden under dem ”levende”. De tre stoffer er uran-238 (halveringstid = 4.5 milliarder år), uran-235 (halveringstid = 700 millioner år) og thorium-232 (halveringstid = 14 milliarder år).
Den fjerde kæde har ikke en flaskehals-isotop der holder så længe, så næsten alle isotoperne i denne kæde er henfaldet til nær stabiltet i enden af kæden.
Nær enden af denne kæde er bismuth-209, der længe blev anset for stabil. For nylig har man dog fundet at Bi-209 er ustabil med en halveringstid på 19 milliarder milliarder år.
Det er det sidste trin før stabilt thallium-205. Omkring den tid hvor solsystemet blev dannet, var der flere ustabile isotoper med høje masser tilstede, og kæderne var længere og indeholdt isotoper der nu er henfaldet. I dag har vi frembragt isotoper, som ellers var henfaldet : plutonium-239, brugt til atomvåben er et godt eksempel med en halveringstid på 24500 år, det henfalder ved udsendelse af alfa-partikler til uran-235.
Typer af henfald
De 4 mest almindelige typer af radioaktive henfald er: alfahenfald, betahenfald, gammahenfald, inverst beta henfald (idet man medregner både positron emission, elektronindfangning), .
Alfa-henfaldet sker ved udsendelse af helium-4 (alfa partikler er helium-4 kerner) og er den eneste af processerne som ændrer atommasse tallet (A) for kernen. Massetallet mindskes med 4 ved et alfa-henfald og på grund af dette, vil næsten ethvert henfald resultere i en kerne, hvis atommasse kan skrives som enten 4n, 4n+1, 4n+2 eller 4n+3, hvilket inddeler nukliderne i fire henfaldskæder.
Tre hoved-henfaldskæder findes i naturen, de kaldes ofte thorium serien, radium serien eller uran serien, og actiniumserien. De repræsenterer tre af de fire omtalte klasser og ender i tre forskellige stabile isotoper af bly.
Massetallene af isotoperne kan repræsenteres ved henholdsvis A = 4n, A = 4n + 2, og A = 4n + 3.
De lang-livede isotoper i toppen af disse kæder, som er henholdsvis thorium-232, uran-238, and uran-235, har eksisteret siden jordens dannelse.
På grund af den forholdsvis korte halveringstid af dens start-isotop neptunium-237 (2.14 millioner år), er den fjerde kæde, kaldet neptunium serien med A = 4n + 1, allerede forsvundet i naturen, bortset fra det sidste trin, henfaldet af bismuth-209.
Slutningen af denne henfaldskæde vides nu at være thallium-205.
Nogle ældre kilder angiver den endelige isotop til at være bismuth-209, men det blev opdaget for nylig, at den har en halveringstid på 1.9×1019 år.
Der er også ikke-transurane henfaldskæder, for eksempel magnesium-28 og chlorine-39. På Jorden er de fleste start-isotoper i disse kæder fra før 1945 frembragt af kosmisk stråling.
Efter 1945 har test af nukleare våben også frigjort talrige radioaktive fission products. Næsten alle sådanne isotoper henfalder enten med beta - eller beta+ henfald, idet de skifter fra et grundstof til et andet uden at ændre masse. Disse datterprodukter har generelt længere halveringstider, da de er tættere på stabilitet og kæden ender med en stabil isotop.
Actiniders alfa-henfaldskæder
I de fire tabeller herunder, er de mindre forgreninger (med forgrenings-sandsynlighed mindre end 0.0001 %) udeladt. Den frigjorte energi udgøres af den totale kinetiske energi af alle de udsendte partikler. (elektroner, alfa partikler, gammakvanter, neutrinoer, Auger electroner og röntgenstråler) og den rekylerende kerne, idet det antages at kernen var i hvile fra start. Bogstavet 'a' betyder år, fra latin annus).
I tabellerne herunder (undtaget for neptunium), er de historiske navne for de naturligt forekommende nuklider også givet. Disse navne var i brug på den tid, da henfaldet først blev opdaget og undersøgt. Fra de historiske navne kan man lokalisere den bestemte kæde som kernen tilhører, og erstatte det med dets moderne navn.
De tre naturligt forekommende aktinid alfahenfaldskæder som er vist herunder - thorium, uran/radium (fra U-238) og actinium (fra U-235) - ender hver i deres bestemte bly-isotop (henholdsvis Pb-208, Pb-206 og Pb-207).
Alle disse isotoper er stabile og er også tilstede i naturen som primordiale nuklider, men den større mængde af dem sammenlignet med bly-204 (som kun har en primordial oprindelse) kan bruges til at aldersbestemme klippe med uranium-lead dating metoden.
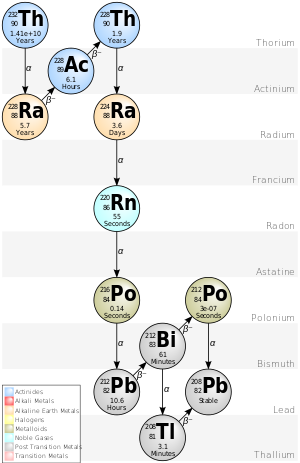
Thorium serien
4n kæden, som begynder med naturligt forekommende thorium-232, indeholder følgende grundstoffer: actinium, bismuth, bly, polonium, radium, radon and thallium. Alle er tilstede, i det mindste midlertidigt, i enhver prøve som indeholder thorium, enten det er et metal, compound, eller et mineral. Serien slutter med bly-208.
Den totale energi som frigøres fra thorium-232 til bly-208, inklusive neutrinoernes energi, er 42.6 MeV
| nuklid | historisk navn (kort) | historisk navn (lang) | henfaldstype | halveringstid (a=år) | frigjort energi, MeV | henfaldsprodukt |
|---|---|---|---|---|---|---|
| 252 | α | 2.645 a | 6.1181 | 248 | ||
| 248Cm | α | 3.4×105 a | 5.162 | 244 | ||
| 244Pu | α | 8×107 a | 4.589 | 240 | ||
| 240U | β− | 14.1 h | .39 | 240 | ||
| 240Np | β− | 1.032 h | 2.2 | 240 | ||
| 240Pu | α | 6561 a | 5.1683 | 236 | ||
| 236U | α | 2.3×107 a | 4.494 | 232 | ||
| 232Th | Th | Thorium | α | 1.405×1010 a | 4.081 | 228 |
| 228Ra | MsTh1 | Mesothorium 1 | β− | 5.75 a | 0.046 | 228 |
| 228Ac | MsTh2 | Mesothorium 2 | β− | 6.25 h | 2.124 | 228 |
| 228Th | RdTh | Radiothorium | α | 1.9116 a | 5.520 | 224 |
| 224Ra | ThX | Thorium X | α | 3.6319 d | 5.789 | 220 |
| 220Rn | Tn | Thoron, Thorium Emanation | α | 55.6 s | 6.404 | 216 |
| 216Po | ThA | Thorium A | α | 0.145 s | 6.906 | 212 |
| 212Pb | ThB | Thorium B | β− | 10.64 h | 0.570 | 212Bi |
| 212Bi | ThC | Thorium C | β− 64.06% α 35.94% | 60.55 min | 2.252 6.208 | 212 208 |
| 212Po | ThC′ | Thorium C′ | α | 299 ns | 8.955 | 208 |
| 208Tl | ThC″ | Thorium C″ | β− | 3.053 min | 4.999 | 208Pb |
| 208Pb | ThD | Thorium D | stabil | . | . | . |
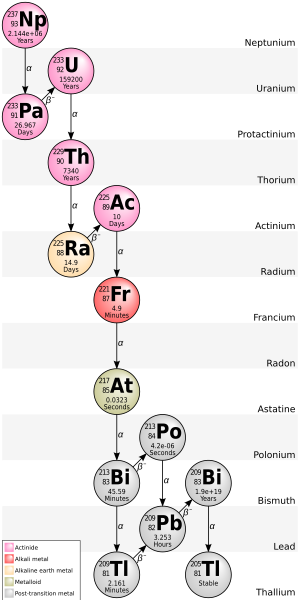
Neptunium serien
4n+1 kæden, der starter med Np-237 kaldes ofte “neptunium serien” eller “neptunium kaskaden”. I denne serie, er det kun 2 af isotoperne som forekommer naturligt, nemlig de sidste to: bismuth-209 og thallium-205.
En røgalarm , som indeholder et americium-241 ioniserings-kammer samler en betydelig mængde af neptunium-237 som henfaldsprodukt af americium: de følgende grundstoffer er også tilstede, i det mindste midlertidigt, som henfaldsprodukter fra neptunium: actinium, astat, bismuth, francium, bly, polonium, protactinium, radium,thallium, thorium, og uran. Da studiet af denne henfaldskæde er af nyere dato har dets nuklider ingen historiske navne. En unik egenskab ved denne kæde er at den ikke omfatter ædelgassen radon. I de andre henfaldskæder er der radon, som kan migrere gennem klipper. Den totale frigjorte energi fra californium-249 til thallium-205, inklusive neutrinoernes energi, er 66.8 MeV.
| nuklid | henfalds type | halveringstid (a=år) | frigjort energi, MeV | henfalds produkt |
|---|---|---|---|---|
| 249 | α | 351 a | 5.813+.388 | 245 |
| 245Cm | α | 8500 a | 5.362+.175 | 241 |
| 241Pu | β− | 14.4 a | 0.021 | 241 |
| 241Am | α | 432.7 a | 5.638 | 237 |
| 237Np | α | 2.14•106 a | 4.959 | 233 |
| 233Pa | β− | 27.0 d | 0.571 | 233 |
| 233U | α | 1.592•105 a | 4.909 | 229 |
| 229Th | α | 7340 a | 5.168 | 225 |
| 225Ra | β− | 14.9 d | 0.36 | 225 |
| 225Ac | α | 10.0 d | 5.935 | 221 |
| 221Fr | α | 4.8 min | 6.3 | 217 |
| 217At | α | 32 ms | 7.0 | 213 |
| 213Bi | β− 97.80% α 2.20% | 46.5 min | 1.423 5.87 | 213 209 |
| 213Po | α | 3.72 μs | 8.536 | 209Pb |
| 209Tl | β− | 2.2 min | 3.99 | 209 |
| 209Pb | β− | 3.25 h | 0.644 | 209 |
| 209Bi | α | 1.9•1019 a | 3.137 | 205 |
| 205Tl | . | stabil | . | . |
Uran serien
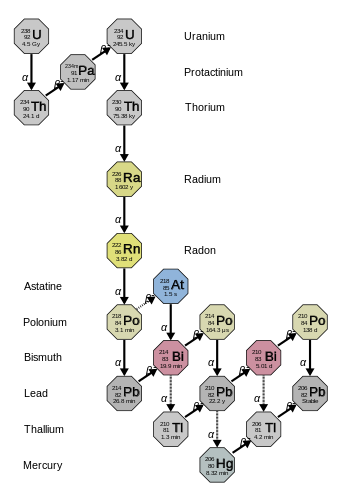
4n+2 henfaldskæden, som starter med naturligt forekommende uran-238, indeholder følgende grundstoffer: astat, bismuth, bly, polonium, protactinium, radium, radon, thallium, og thorium. Alle disse er tilstede, i det mindste midlertidigt, i enhver prøve som indeholder uran-238. Serien slutter med bly-206.
Den totale energi som frigøres fra uran-238 til bly-206, inklusive neutrinoernes energi, er 51.7 MeV
Actinium serien
4n+3 henfaldskæden,som starter med naturligt forekommede U-235, indeholder følgende grundstoffer: actinium, astat, bismuth, francium, bly, polonium, protactinium, radium, radon, thallium, og thorium. Alle er tilstede, i det mindste midlertidigt, i enhver prøve indeholdende uran-235. Serien slutter med den stabile isotop Bly-207.
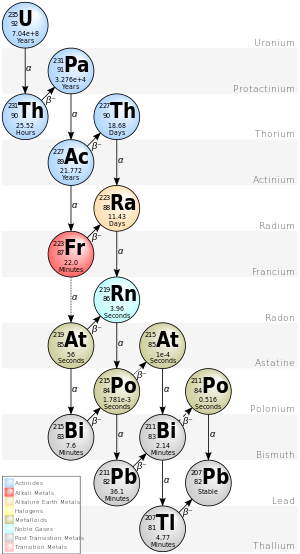
Den totale energi som frigøres fra uran-235 til bly-207, inklusive neutrinoernes energi, er 46.4 MeV
| nuklid | historisk navn (kort) | historisk navn (langt) | henfalds-type | halveringstid (a=år) | frigjort energi, MeV | henfaldsprodukt |
|---|---|---|---|---|---|---|
| 239Pu | α | 2.41•104 a | 5.244 | 235U | ||
| 235U | AcU | Actin Uran | α | 7.04•108 a | 4.678 | 231 |
| 231Th | UY | Uran Y | β− | 25.52 h | 0.391 | 231 |
| 231Pa | Protactinium | α | 32760 a | 5.150 | 227 | |
| 227Ac | Ac | Actinium | β− 98.62% α 1.38% | 21.772 a | 0.045 5.042 | 227 223 |
| 227Th | RdAc | Radioactinium | α | 18.68 d | 6.147 | 223 |
| 223Fr | AcK | Actinium K | β− 99.994% α 0.006% | 22.00 min | 1.149 5.340 | 223Ra 219 |
| 223Ra | AcX | Actinium X | α | 11.43 d | 5.979 | 219 |
| 219At | α 97.00% β− 3.00% | 56 s | 6.275 1.700 | 215 219Rn | ||
| 219Rn | An | Actinon, Actinium Emanation | α | 3.96 s | 6.946 | 215 |
| 215Bi | β− | 7.6 min | 2.250 | 215Po | ||
| 215Po | AcA | Actinium A | α 99.99977% β− 0.00023% | 1.781 ms | 7.527 0.715 | 211 215 |
| 215At | α | 0.1 ms | 8.178 | 211 | ||
| 211Pb | AcB | Actinium B | β− | 36.1 min | 1.367 | 211Bi |
| 211Bi | AcC | Actinium C | α 99.724% β− 0.276% | 2.14 min | 6.751 0.575 | 207 211 |
| 211Po | AcC' | Actinium C' | α | 516 ms | 7.595 | 207 |
| 207Tl | AcC" | Actinium C" | β− | 4.77 min | 1.418 | 207Pb |
| 207Pb | AcD | Actinium D | . | stabilt | . | . |
Beta-henfaldskæder i fissionsprodukter
Da de tunge oprindelige kerner altid har en større andel af neutroner, starter fissionsprodukt-kerner næsten altid med et neutron/proton-forhold, der er væsentligt større end det, der er stabilt i deres masseinterval. De gennemgår derfor flere betahenfald efter hinanden, hver konverterer en neutron til en proton. De første henfald tenderer til at have højere henfaldsenergi og kortere halveringstid. Disse sidste henfald kan have lav henfaldsenergi og/eller lang halveringstid.
Eksempelvis har uran-235 92 protoner og 143 neutroner. Fission tager en ekstra neutron, og producerer så to eller tre neutroner mere; antag at 92 protoner og 142 neutroner er tilgængelige for de to fissionsprodukt-kerner. Antag, at de har massen 99 med 39 protoner og 60 neutroner (yttrium-99), og massen 135 med 53 protoner og 82 neutroner (iod-135); i så fald kan henfaldskæden ses af nedenstående oversigt.
| Kerne | Halveringstid |
|---|---|
| 99 | 1.470(7) s |
| 99 | 2.1(1) s |
| 99m | 2.6(2) min |
| 99 | 15.0(2) s |
| 99m2 | 0.76(6) µs |
| 99m1 | 15.5(2) µs |
| 99 | 2.7489(6) d |
| 99m | 6.0058(12) h |
| 99Tc | 2.111(12)E+5 a |
| 99 | stabil |
| Kerne | Halveringstid |
|---|---|
| 135 | 6.57(2) h |
| 135 | 9.14(2) h |
| 135 | 2.3(3)E+6 a |
| 135 | stabil |
Noter
Litteratur
- C.M. Lederer, J.M. Hollander, I. Perlman (1968). Table of Isotopes (6th udgave). New York: John Wiley & Sons.
{{cite book}}: CS1-vedligeholdelse: Flere navne: authors list (link)
Eksterne henvisninger
- Nucleonica nuclear science portal
- Nucleonica's Decay Engine for professional online decay calculations
- Decay chains
- Government website listing isotopes and decay energies Arkiveret 5. december 2006 hos Wayback Machine
- National Nuclear Data Center Freely available databases that can be used to check or construct decay chains. Fully referenced.
 The Live Chart of Nuclides - IAEA with decay chains
The Live Chart of Nuclides - IAEA with decay chains- Decay Chain Finder
|
Medier brugt på denne side
icon for the live chart of nuclides application at the IAEA Nuclear Data Section
Forfatter/Opretter: http://commons.wikimedia.org/wiki/User:BatesIsBack, Licens: CC BY-SA 3.0
A modification of the original image to fix the half-life of Pb-212.
Forfatter/Opretter: Edgar Bonet, Licens: CC BY-SA 3.0
Decay chain 4n+3: Actinium series. Dashed arrow is a decay mode with < 1% probability. Dotted arrows are decay modes with < 0.01% probability.
Forfatter/Opretter: User:Tosaka, Licens: CC BY 3.0
Uranium-238 decay chain diagram
Forfatter/Opretter: User:Johantheghost, Licens: CC BY-SA 3.0
A diagram illustrating the radioactive decay chains of the non-synthetic elements.
The four decay chains shown are
- thorium (in blue);
- radium (in red);
- actinium (in green); and
- neptunium (in purple).
Forfatter/Opretter:
Decay chain 4n+1, Neptunium series.