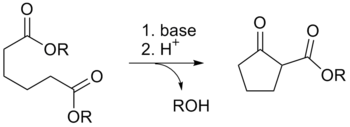Dieckmann-kondensation
En Dieckmann-kondensation er en intramolekylær kemisk reaktion mellem diestre med en base til at give β-ketoestere.[1][2][3][4][5] Reaktionen er opkaldt efter den tyske kemiker Walter Dieckmann (1869–1925). Den ækvivalente intermolekylære reaktion er Claisen-kondensation.
Reaktionsmekanisme
Det sure hydrogen mellem to carbonylgrupper bliver deprotoniseret i fjerde trin. Protoniseringen med en Brønsted-Lowry-syre (H3O+ for eksempel) gendanner β-keto esteren.[6] Deprotoniseringstrinnet er drivkraften i reaktionen.
Grundet den steriske stabilitet af fem- og seksleddede ringstrukturer, bliver disse fortrinsvist dannet. 1,4- og 1,6 diestere danner femleddede cykliske β-keto estere, mens 1,5- og 1,7 diestere vil danne seksleddede β-keto estere.[7]
 |
| Animation |
Se også
- Claisen-kondensation
- Gabriel-Colman omlejring
Referencer
- ^ Dieckmann, W. Ber. 1894, 27, 102 & 965
- ^ Dieckmann, W. Ber. 1900, 33, 595 & 2670
- ^ Dieckmann, W. Ann. 1901, 317, 51 & 93
- ^ Schaefer, J. P.; Bloomfield, J. J. (1967). "The Dieckmann Condensation (Including the Thorpe-Ziegler Condensation)". Organic Reactions. 15: 1-203. doi:10.1002/0471264180.or015.01.
- ^ Davis, B. R.; Garrett, P. J. Comp. Org. Syn. 1991, 2, 806-829. (Review)
- ^ Janice Gorzynski Smith (2007). Organic Chemistry (2nd udgave). s. 932–933. ISBN 978-0073327495.
- ^ "Dieckmann Condensation". Organic Chemistry Portal. Arkiveret fra originalen 1. august 2014. Hentet 19. juni 2014.
Medier brugt på denne side
Forfatter/Opretter: Kus2014, Licens: CC BY-SA 4.0
An animation of the reaction mechanism of the Dieckmann condensation
Dieckmann condensation mechanism
Dieckmann condensation