Bohrium
| Bohrium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Periodiske system | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Generelt | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomtegn | Bh | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomnummer | 107 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
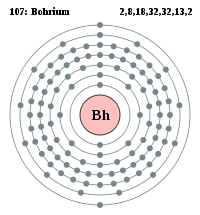
| Elektronkonfiguration | 2, 8, 18, 32, 32, 13, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppe | 7 (Overgangsmetal) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | 7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-nummer | 54037-14-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomare egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | (264) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronkonfiguration | [Rn] 5f14 6d5 7s² (gæt baseret på rhenium) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroner i hver skal | 2, 8, 18, 32, 32, 13, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidationstrin | 7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fysiske egenskaber | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tilstandsform | Formentlig fast stof | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Bohrium (opkaldt efter Niels Bohr) er det 107. grundstof i det periodiske system, og har det kemiske symbol Bh: Dette radioaktive overgangsmetal findes ikke i naturen, men fremstilles kunstigt i uhyre små mængder i laboratorier.
Egenskaber
Man kan kun fremstille ganske små mængder af bohrium og tilsvarende tunge grundstoffer ad gangen, og det besværliggør undersøgelser af disse stoffers kemiske egenskaber. Kemiske forsøg udført i 2000 på isotopen 267Bh viser at bohrium reagerer med ilt og saltsyre under dannelse af bohriumoxyklorid, på en måde der "matcher" andre stoffer fra gruppe 7; rhenium og technetium.
Fremstilling af bohrium
Da alle isotoper af Bohrium har ganske korte halveringstider (273Bh og 274Bh har rekorden med blot ca. halvanden time), eksisterer stoffet ikke i naturen. I laboratoriet er der to måder at fremstille det på; i begge tilfælde accelereres en ion af et forholdsvis let grundstof som krom eller mangan mod et "mål" af et temmelig tungt grundstof, for eksempel bly eller vismut. Ved kollisionen fusioneres ("sammenføjes") de lette og tunge atomkerner, enten med en bohriumisotop som resultat, eller også skabes et andet meget tungt grundstof, som hurtigt henfalder til en bohriumisotop.
Historie
Dmitrij Mendelejev havde i sit periodiske system en "tom plads" neden under rhenium, som han navngav eka-rhenium. Stoffet blev første gang fremstillet i 1976 af et sovjetisk forskninghold ledet af Ju. Oganessian på Instituttet for Atomforskning ved Dubna, som skabte isotopen Bh-261 med en halveringstid på 1-2 ms (senere data angav en halveringstid på omkring 10 ms). De skabte Bh ved at skyde en kerne af krom-24 imod bismuth-204.
I 1981 bekræftede et tysk forskningshold under ledelse af Peter Armbruster og Gottfried Münzenberg ved Gesellschaft für Schwerionenforschung (Institutet for Tung Ion Forskning) i Darmstadt det sovjetiske holds resultater og producerede Bohrium, men denne gang Bh-262 med længere levetid.
Tyskerne foreslog at navngive det nyfundne stof nielsbohrium til ære for den danske fysiker Niels Bohr. De sovjetiske forskere havde foreslået navnet til grundstof 105 (dubnium).
IUPAC (International Union of Pure and Applied Chemistry) navngav i første omgang stoffet som Unnilseptium (Uns). I 1984 anbefalede en komité nedsat af IUPAC at elementet kom til at hedde Bohrium. Skønt mange protesterede over at navnet kunne forveksles med Bor, blev det godkendt i 1997.
Isotoper af bohrium
Man kender 16 isotoper af bohrium, som alle er radioaktive. Generelt har de tungeste isotoper længst levetid; efter 273Bh og 274Bh har 275Bh den længste halveringstid; omkring 40 minutter. Alle andre isotoper, fra 260Bh til 272Bh, er lettere men har kortere halveringstider.
Eksterne henvisninger
 | Wikimedia Commons har medier relateret til: |
- WebElements.com – Bohrium
- Apsidium – Bohrium Arkiveret 25. oktober 2005 hos Wayback Machine
- Los Alamos National Laboratory – Bohrium Arkiveret 12. december 2010 hos Wayback Machine
|
Medier brugt på denne side
(c) Peo at the Danish language Wikipedia, CC BY-SA 3.0
Denne tegning forestiller elektronkonfigurationen i et bohriumatom: Den store kugle i midten forestiller atomkernen, og de små kugler er elektronerne. Bogstaverne på elektron-kuglerne angiver hvilken orbital de tilhører. Den lyserøde farve markerer at bohrium hører til overgangsmetallerne. Udarbejdet af Peo, og frigivet under samme GFDL-betingelser som Wikipedia som helhed.
Forfatter/Opretter: Pumbaa (original work by Greg Robson), Licens: CC BY-SA 2.0 uk
Electron shell diagram for Bohrium, the 107th element in the periodic table of elements.

