Alkohol (stofklasse)
 For alternative betydninger, se Alkohol. (Se også artikler, som begynder med Alkohol)
For alternative betydninger, se Alkohol. (Se også artikler, som begynder med Alkohol)
Alkoholer (eller evt. alkanoler) er i organisk kemi en fællesbetegnelse for kemiske forbindelser, der har en hydroxylgruppe (dvs. en OH-gruppe), der er bundet kovalent til et kulstofatom.
Kemiske forbindelser med en OH-gruppe bundet til et aromatisk C-atom kaldes phenoler og betragtes ikke som alkoholer.
Struktur
Alkoholerne inddeles i tre kategorier:
- Primære alkoholer, hvor OH-gruppen er bundet til et C-atom, der kun er bundet til højst ét andet C-atom, dvs. indeholder strukturen -CH2OH.
Generel formel for primære alkoholer:
- Sekundære alkoholer, hvor OH-gruppen er bundet til et C-atom, der er bundet til netop to andre C-atomer, dvs. indeholder strukturen >CHOH.
Generel formel for sekundære alkoholer:
- Tertiære alkoholer, hvor OH-gruppen er bundet til et C-atom, der er bundet til tre andre C-atomer. En tertiær alkohol indeholder atomgruppen COH.
Generel formel for tertiære alkoholer:
En alkohol med mere end én OH-gruppe kan falde inden for flere af ovennævnte kategorier. Et godt eksempel er glycerol, der indeholder tre OH-grupper – to primære og en sekundær.
Kemiske egenskaber
Alkoholer er meget svage syrer (svagere end vand) med en pKs på 24.[1]
Ved kondensation af en alkohol med en carboxylsyre, et anhydrid eller et syrechlorid dannes der en ester.
Alkoholer er moderat stærke nukleofiler. Ved nucleofil substitution af et organisk halogenid med en alkohol dannes en ether.
Under syrekatalyse kan alkoholer eliminere vand under dannelse af alkener. Tertiære alkoholer eliminerer hurtigere end sekundære, som igen er hurtigere end primære.
Fysiske egenskaber
Fysiske egenskaber for nogle alkoholer:
| Alkohol | Smeltepunkt | Kogepunkt | Opløselighed i vand (20 °C) |
|---|---|---|---|
| Methanol | -98 °C | 65 °C | Fuldstændigt opløseligt |
| Ethanol | -117 °C | 78,29 °C | Fuldstændigt opløseligt |
| Propan-1-ol | -126 °C | 97 °C | Fuldstændigt opløseligt |
| Propan-2-ol | -90 °C | 82 °C | Fuldstændigt opløseligt |
| Butan-1-ol | -90 °C | 118 °C | 7,4 g per 100 mL vand |
| Pentan-1-ol | -79 °C | 138 °C | 2,7 g per 100 mL vand |
Eksempler på alkoholer
| CH3–CH2–CH2–OH |  |  |  | 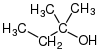 |
 | 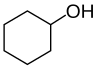 | 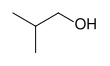 | ||
| n-propyl alcohol, propan-1-ol, eller 1-propanol | isopropyl alcohol, propan-2-ol, eller 2-propanol | cyclohexanol | isobutyl alcohol, 2-methylpropan-1-ol, eller 2-methyl-1-propanol | tert-amyl alcohol, 2-methylbutan-2-ol, eller 2-methyl-2-butanol |
| en primær alkohol | en sekundær alkohol | en sekundær alkohol | en primær alkohol | en tertiær alkohol |
- Metanol (træsprit) er en primær alkohol.
- Ætanol/Ethanol (sprit) er en primær alkohol.
- Isopropylalkohol, (isopropanol) er en sekundær alkohol.
- Glycerol er både en primær og en sekundær alkohol.
- Mælkesyre er en sekundær alkohol (og en carboxylsyre).
Følgende regler gælder for navngivning af alkoholer:
- Find molekylets længste carbonkæde, der indeholder C-atomet med hydroxygruppen, og bestem navnet på den tilsvarende alkan.
- Nummerer C-atomerne i carbonkæden, så C-atomet med hydroxygruppen får lavest muligt nummer.
- Tilføj nummeret på C-atomet med hydroxygruppen og endelsen -ol til alkannavnet.
- Ved en forgrening angives sidekædernes placering og navne i alfabetisk rækkefølge forrest i navnet.
- Er der to, tre eller fire ens sidegrupper bundet til carbonkæden, angives de med forstavelserne di-, tri- eller tetra-. Disse forstavelser indgår ikke i alfabetiseringen.
Se også
Referencer
Ekstern henvisning
 | Wikimedia Commons har medier relateret til: |
- Kennesaw State University: Alkoholernes kemi og kendetegn Arkiveret 4. april 2005 hos Wayback Machine (engelsk)
- Sundhed-EU-portal – Alkohol
Medier brugt på denne side
Forfatter/Opretter: Jonasfolmer, Licens: CC BY-SA 4.0
Generel formel for sekundære alkoholer
chemical structure of propan-1-ol, made using BKchem
Chemical structure of cyclohexanol.
Chemical stucture of isobutanol, made using BKchem
Forfatter/Opretter: Jonasfolmer, Licens: CC BY-SA 4.0
Generel formel for tertiær alkoholer:
Displayed formula of cyclohexanol, for clarity in elementary chemistry.
Displayed formula of 2-methylpropan-1-ol (isobutanol), for clarity in elementary chemistry.
Displayed formula of propan-2-ol (isopropanol), for clarity in elementary chemistry.
Strukturformel von 2-Methyl-2-butanol
Forfatter/Opretter: Jonasfolmer, Licens: CC BY-SA 4.0
Generel formel for et primært alkohol
2-Propanol; Isopropanol
Forfatter/Opretter: User:GKFX, based on work by User:Jü, Licens: CC BY-SA 4.0
Displayed formula of 2-methylbutan-2-ol, for clarity in elementary chemistry.














